- Реферат.Справочник
- Контрольные работы по химии
- Эндотермическая реакция взаимодействия метана с диоксидом углерода протекает по уравнению
Условие
Эндотермическая реакция взаимодействия метана с диоксидом углерода протекает по уравнению CH4(г) + CO2 = 2CO(г) + 2H2(г); ΔH = +247,37 кДж. При какой температуре начнется эта реакция? Дано: ΔH = 247,37 кДж S⁰(CH4(г)) =186,2Джмоль*К S⁰(CO2(г))= 213,5Джмоль*К S⁰(CО(г)) =197,6Джмоль*К S⁰( H2(г)) =130,6Джмоль*К
Ответ
реакция начнется при температуре 963,7К
Решение
CH4(г) + CO2 = 2CO(г) + 2H2(г) Т = ΔHΔS ΔS = ƩS⁰прод — ƩS⁰исх.= = (2 * S⁰( CO2(г)) + 2 * S⁰( H2(г))) – (S⁰(CH4(г)) + S⁰( CO2(г))) ΔS = (2 * 197,6 + 2 * 130,6) – (186,2 + 213,5) = =256,7 Дж/моль*К = 0,2567 кДж/моль*К Т = 247,370,2567 = 963,7 К Следовательно, реакция начнется при температуре 963,7К Ответ: реакция начнется при температуре 963,7К
Эндотермическая реакция взаимодействия метана с оксидом углерода (IV) протекает по уравнению CH4(г)+CO2(г)=2CO(г)+2H2(г); ΔH298
Ваш ответ
решение вопроса
Похожие вопросы
- Все категории
- экономические 43,399
- гуманитарные 33,632
- юридические 17,905
- школьный раздел 607,960
- разное 16,854
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Примеры решения задач по Химии
| 1. Эндотермическая реакция взаимодействия метана с диоксидом углерода протекает по уравнению CH4(г) + СO2(г) = 2СО(г) + 2Н2(г); ?Н = +247,37 кДж. При какой температуре начнется эта реакция? |
Решение
CH4(г) + СO2(г) = 2СО(г) + 2Н2(г); Н = +247,37 кДж.
DS =( 197,9 х2 + 130,59х2) – 186,19 + 213,65 = 257,14 Дж
Вычисляем DGo реакции:
DG = DH – TDS = 247,37 – 298 257,14= +55,28 кДж.
Так как DG > 0, то реакция при стандартных условиях невозможна; наоборот, при этих условиях идет обратная реакция
Найдем температуру, при которой DG = 0:
Т = ?Н / ?S = 247,37 / 0,257 =961,9 K.
Следовательно, при температуре » 961,9 K начнется реакция .
уравнением:
CH3OH(ж) + 1?O2(г) = CO2(г) + 2H2O(ж); ?H = ?
Вычислите тепловой эффект этой реакции, если известно, что мольная теплота парообразования CH3OH(ж) равна
+ 37,4 кДж.
Решение
?H(СН3ОН(ж.)) = -238,7 кДж/моль
?Н(Н2O(ж.)) = -285,84 кДж/моль
?Н(СО2(г.)) = -393,51 кДж/моль
?Н(О2) = 0
?Н(общ.) = Н(прод.) — Н(исх.) = (-393,51) + 2*(-285,84) + 238,7 = -726,49 кДж
а) 6,02•1022 молекул С2Н2;
б) 1,8•1024 атомов азота;
в) 3,01•1023 молекул NН3.
Какова мольная масса указанных веществ.
Решение
Моль — это такое количество вещества (или его порция), которое содержит 6,02 • 1023 (округленно 6 · 1023 частиц (молекул, атомов или других частиц).
NA= 6,02 • 1023 моль-1 = 6,02 • 1023
n = N / NA
а) 6,02•1022 молекул С2Н2;
n =6,02•1022/ 6,02 • 1023=0,1 моль
б) 1,8•1024 атомов азота;
n =1,8•1024 /6,02 • 1023= 2,9 моль
в) 3,01•1023 молекул NН3.
n =3,01•1023 /6,02 • 1023= 0,5 моль
Решение.
Эквивалентные массы вычисляются по закону эквивалентов, который математически может быть выражен зависимостью:
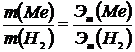
где 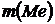
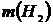
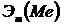
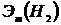
Если одно из веществ находится в газообразном состоянии, то, как правило, его количество измеряется в объемных единицах. Поэтому целесообразно воспользоваться следующей зависимостью:
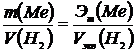
В результате получаем:
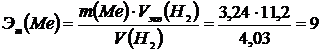
Аг = 9·3 = 27.
Решение
Квантовые числа – энергетические параметры, определяющие состояние электрона и тип атомной орбитали, на которой он находится.
Главное квaнтовое число n определяет общую энергию электрона и степень его удаления от ядра (номер энергетического уровня); оно принимает любые целочисленные значения, начиная с 1 (n = 1, 2, 3, . . .)
Орбитальное (побочное или азимутальное) квантовое число l определяет форму атомной орбитали. Оно может принимать целочисленные значения от 0 до n-1 (l = 0, 1, 2, 3,…, n-1). Каждому значению lсоответствует орбиталь особой формы. Орбитали с l = 0 называются s-орбиталями,
l = 1 – р-орбиталями (3 типа, отличающихся магнитным квантовым числом m), l = 2 – d-орбиталями (5 типов), l = 3 – f-орбиталями (7 типов).
Магнитное квантовое число mопределяет ориентацию орбитали в пространстве относительно внешнего магнитного или электрического поля. Его значения изменяются от +l до -l, включая 0. Например, при l = 1 число mпринимает 3 значения: +1, 0, -1, поэтому существуют 3 типа р-АО:  рx, рy, рz.
Спиновое квантовое число s может принимать лишь два возможных значения +1/2 и -1/2. Они соответствуют двум возможным и противоположным друг другу направлениям собственного магнитного момента электрона, называемого спином (от англ. веретено). Для обозначения электронов с различными спинами используются символы: ^ и v.



