- We are checking your browser. gomolog.ru
- Why do I have to complete a CAPTCHA?
- What can I do to prevent this in the future?
- И электродные реакции для некоторых металлов
- Электролиз
- Электролиз
- Электролиз растворов
- Катодные процессы
- Анодные процессы
- Суммарные процессы электролиза
- Электролиз расплавов
- Электролиз с растворимыми электродами
We are checking your browser. gomolog.ru
Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Cloudflare Ray ID: 6de593de9fa50c36 • Your IP : 85.95.188.35 • Performance & security by Cloudflare
И электродные реакции для некоторых металлов
| Электрод | Электродная реакция | j o , В | Электрод | Электродная реакция | j o , В |
| Li + /Li | Li + + ē = Li | –3,045 | Cd 2+ /Cd | Cd 2+ + 2ē = Cd | –0,403 |
| Rb + /Rb | Rb + + ē = Rb | –2,925 | Co 2+ /Co | Co 2+ + 2ē = Co | –0,277 |
| K + /K | K + + ē = K | –2,924 | Ni 2+ /Ni | Ni 2+ + 2ē = Ni | –0,250 |
| Cs + /Cs | Cs + + ē = Cs | –2,923 | Sn 2+ /Sn | Sn 2+ + 2ē = Sn | –0,136 |
| Ba 2+ /Ba | Ba 2+ + 2ē = Ba | –2,906 | Pb 2+ /Pb | Pb 2+ + 2ē = Pb | –0,126 |
| Ca 2+ /Ca | Ca 2+ + 2ē = Ca | –2,866 | Fe 3+ /Fe | Fe 3+ + 3ē = Fe | –0,036 |
| Na + /Na | Na + + ē = Na | –2,714 | 2H + /H2 | 2H + + 2ē = H2 | 0,000 |
| Mg 2+ /Mg | Mg 2+ + 2ē = Mg | –2,363 | Bi 3+ /Bi | Bi 3+ + 3ē = Bi | +0,215 |
| A1 3+ /A1 | Al 3+ + 3ē = Al | –1,662 | Cu 2+ /Cu | Cu 2+ + 2ē = Cu | +0,337 |
| Ti 2+ /Ti | Ti 2+ + 2ē = Ti | –1,628 | Ag + /Ag | Ag + + ē = Ag | +0,799 |
| Mn 2+ /Mn | Mn 2+ + 2ē = Mn | –1,180 | Hg 2+ /Hg | Hg 2+ + 2ē = Hg | +0,854 |
| Zn 2+ /Zn | Zn 2+ + 2ē = Zn | –0,763 | Pt 2+ /Pt | Pt 2+ + 2ē = Pt | +1,190 |
| Cr 3+ /Cr | Cr 3+ + 3ē = Cr | –0,744 | Au 3+ /Au | Au 3+ + 3ē = Au | +1,498 |
| Fe 2+ /Fe | Fe 2+ + 2ē = Fe | –0,440 | Au + /Au | Au + + ē = Au | +1,691 |
Расположенные в порядке увеличения стандартного электродного потенциала металлы образуют ряд напряжений металлов. Положение металла в ряду напряжений определяет относительную окислительно-восстановительную способность металла и его ионов. Чем меньшее значение имеет стандартный электродный потенциал металла, тем более сильным восстановителем он является. Чем больше потенциал металлического электрода, тем более высокой окислительной способностью обладают его ионы. Каждый металл способен вытеснять из растворов солей только те металлы, которые имеют большее значение электродного потенциала – более активный металл замещает менее активный.
Последовательность металлов в ряду напряжений сохраняется только для стандартной температуры (25 °С) и концентрации ионов металла в растворе 1моль/л. При других концентрациях электролита электродный потенциал рассчитывается по уравнению Нернста:
j = j 0 + 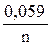
где j 0 − стандартный электродный потенциал, n – число электронов, участвующих в электродной реакции; C – концентрация ионов металла в растворе (моль/л).
Если два электрода, погруженные в растворы электролитов, соединить металлическим проводником, образуется гальванический элемент. Гальваническими элементаминазывают устройства, в которых химическая энергия окислительно-восстановительных процессов преобразуется в электрическую энергию.
Так, реакция CuSO4 + Zn = Cu + ZnSO4 в электрохимическом варианте является основой гальванического элемента Даниэля – Якоби, схема которого (–) Zn | ZnSO4 || CuSO4 |Cu (+) отражает систему обозначений для гальванических элементов. Слева записывается анод Zn | Zn 2+ – электрод, имеющий меньшее значение электродного потенциала, отрицательный полюс (–), на нем протекает процесс окисления – анодная реакция: Zn –2ē = Zn 2+ . Справа – катод Cu 2+ | Cu – электрод, имеющий большее значение электродного потенциала, положительный полюс (+), на нем протекает процесс восстановления – катодная реакция: Cu 2+ + 2ē = Cu. Одна вертикальная черта изображает фазовый раздел между металлом и раствором электролита. Двойная вертикальная линия отделяет анодное пространство от катодного.
Суммарная реакция, протекающая в гальваническом элементе, называется токообразующей. В случае элемента Даниэля – Якоби токообразующая реакция имеет вид Cu 2+ + Zn = Cu + Zn 2+ .
Максимальная разность потенциалов электродов, которая может быть получена при работе гальванического элемента, называется электродвижущей силой(ЭДС). Обозначается E, измеряется в вольтах. ЭДС элемента равна разности потенциалов катода и анода: E = j к – j а
Стандартная ЭДС равна разности стандартных электродных потенциалов катода и анода:E 0 = j 0 к– j 0 а Так, для элемента Даниэля – Якоби стандартная ЭДС равна: E 0 = j 0 Сu 2+ /Cu – j 0 Zn 2+ /Zn = +0,337 – (–0,763) = +1,100 В.
Окислительно-восстановительная реакция, характеризующая работу гальванического элемента, протекает в направлении, в котором ЭДС имеет положительное значение. В этом случае DG 0 х.р. 0 = – nE 0 F,
где n – число электронов, участвующих в электродной реакции; F – постоянная Фарадея, равная 96500 Кл; E 0 – стандартная ЭДС.
Гальванический элемент, состоящий из двух электродов одного и того же металла, погруженных в растворы его соли разной концентрации, представляет собой концентрационный элемент. В этом случае электрод, погруженный в раствор электролита с меньшей концентрацией ионов металла, будет анодом. В качестве катода будет выступать электрод, опущенный в электролит с большей концентрацией ионов металла.
Пример 12.1.Определить ЭДС концентрационного серебряного элемента с концентрациями ионов серебра, равными 10 –1 моль/л у одного электрода и
10 –4 моль/л у другого при 298 К.
Решение.Схема такого гальванического элемента Ag½Ag + ||Ag + ½Ag. По уравнению Нернста рассчитываем потенциалы двух серебряных электродов.
Для первого электрода:
j Ag + /Ag = j 0 Ag + /Ag + 0,059 lg10 -1 = 0,799 + 0,059×(–1) = 0,74 В
Для второго электрода:
j Ag + /Ag = j 0 Ag + /Ag + 0,059 lg10 -4 = 0,799 + 0,059×(–4) = 0,563 В
Первый электрод с большим значением потенциала в данном элементе является катодом, второй – анодом. ЭДС рассчитываем по формуле:
E = j к – j а = 0,74 – 0,563 = 0,177 В.
Пример 12.2. Рассчитать ЭДС элемента Cd½Cd 2+ || Ni 2+ ½Ni при концентрации ионов Cd 2+ и Ni 2+ , равных соответственно 0,1 и 0,001 моль/л.
Решение.Используя уравнения Нернста и данные таблицы стандартных электродных потенциалов, рассчитываем электродные потенциалы кадмия и никеля:
j Сd 2+ /Cd = j 0 Сd 2+ /Cd + 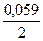
j Ni 2+ /Ni = j 0 Ni 2+ /Ni + 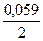
Так как j Сd 2+ /Cd 2+ /Ni , то токообразующей в этом гальваническом элементе является реакция Cd 0 + Ni 2+ = Cd 2+ + Ni 0 . Рассчитываем ЭДС элемента E = j Ni 2+ /Ni – j Сd 2+ /Cd = -0,2795 — (-0,4915) = 0,212 В.
Пример 12.3. Исходя из значений стандартных электродных потенциалов и DG 0 х.р., указать, можно ли в гальваническом элементе осуществить реакцию Pb 2+ + Ti = Pb + Ti 2+ . Составить схему гальванического элемента, написать уравнения электродных реакций.
Решение. В соответствии с уравнением реакции схему гальванического элемента можно представить следующим образом: (–) Ti½Ti 2+ || Pb 2+ ½Pb (+). Уравнения электродных реакций имеют вид:
на аноде: Ti 0 – 2ē ® Ti 2+
на катоде: Pb 2+ + 2ē ® Pb 0
Рассчитываем стандартное значение ЭДС:
Энергию Гиббса рассчитываем по уравнению DG 0 = –nE 0 F=
–2×1,502×96500 = –289,9 кДж. Так как DG 0 2+ + Zn = Cu + Zn 2+
Один моль эквивалентов цинка (32,69 г/моль) будет замещаться на один моль эквивалентов меди (31,77 г/моль) или свинца (103,6 г/моль). Учитывая молярные массы эквивалентов этих элементов, в растворе CuSO4 масса цинковой пластины будет незначительно уменьшаться, а в растворе Pb(NO3)2 – заметно увеличиваться.
Стандартный потенциал магния имеет меньшее значение, чем потенциал цинка. Это означает, что ионы магния не могут окислять цинковую пластинку. Поведение цинка в таком растворе аналогично окислению цинковой пластинки в воде: Zn – 2ē = Zn 2+ . Протекание такого процесса приведет к малозаметному снижению массы цинковой пластинки.
Пример 12.5.Как происходит коррозия цинка, находящегося в контакте с кадмием, во влажном воздухе и в кислом растворе (НСl)? Составить уравнения анодного и катодного процессов. Привести схемы образующихся при этом гальванических элементов. Определить состав продуктов коррозии.
Решение.Цинк имеет меньшее значение потенциала (–0,763 В), чем кадмий (–0,403 В), поэтому он является анодом, а кадмий – катодом. Следовательно, цинк растворяется, а на поверхности кадмия идет восстановление: в кислом растворе – ионов водорода, во влажном воздухе – растворенного в воде кислорода.
Анодный процесс: Zn – 2ē = Zn 2+
Катодный процесс: в кислом растворе 2Н + + 2ē ® Н2
во влажном воздухе О2 + 2Н2О + 4ē ® 4ОН –
Схема образующегося гальванического элемента во влажном воздухе:
Схема образующегося гальванического элемента в кислом растворе:
Во влажном воздухе ионы Zn 2+ с гидроксильными группами, выделяющимися на катоде, образуют малорастворимый гидроксид цинка Zn(ОН)2, который и является продуктом коррозии.
В кислой среде на поверхности кадмия выделяется газообразный водород. В раствор переходят ионы Zn 2+ .
Пример 12.6. Хром находится в контакте с медью. Какой из металлов будет окисляться при коррозии, если эта пара металлов попадает в кислую среду (НС1)? Привести уравнения анодного и катодного процессов, схему образующегося гальванического элемента. Каков состав продуктов коррозии?
Решение.По положению в ряду напряжений металлов видно, что хром более активный металл (j 0 Сr 3+ /Cr = –0,744 В), чем медь (j 0 Сu 2+ /Cu = 0,337 В). В образованной гальванической паре Cr – анод, он окисляется, а Cu – катод, на ее поверхности выделяется (восстанавливается) водород из НС1.
Анодный процесс: Cr –3ē = Cr 3+
Катодный процесс в кислой среде: 2Н + + 2ē ® Н2
Схема гальванического элемента: (–) Cr½HCl½Cu (+)
Появляющиеся ионы Cr 3+ образуют с хлорид-анионами (из НС1) растворимое соединение – CrC13, на поверхности меди выделяется Н2.
Задачи
№ 12.1. а) Чему равна величина ЭДС гальванического элемента, составленного из стандартных цинкового и серебряного электродов, погруженных в растворы их солей? Привести схему гальванического элемента и реакции, протекающие на электродах при его работе. (Ответ: 1,562 В).
б) Возможна ли электрохимическая коррозия алюминия, контактирующего со свинцом в нейтральном водном растворе, содержащем растворенный кислород? Если да, то написать уравнения реакций анодного и катодного процессов. Составить схему образующегося гальванического элемента.
№ 12.2. а) Чему равна величина ЭДС цинкового концентрационного элемента, составленного из двух цинковых электродов, опущенных в растворы с концентрациями ионов Zn 2+ , равными 10 –2 и 10 –6 моль/л? Привести схему такого элемента и реакции, протекающие на электродах при его работе.
б) Как происходит атмосферная коррозия луженого и оцинкованного железа при нарушении покрытия? Составить уравнения анодного и катодного процессов. Привести схемы образующихся гальванических элементов.
№ 12.3. а) Имеется гальванический элемент, в котором протекает токообразующая реакция Ni + Cu 2+ = Cu + Ni 2+ . Привести схему такого элемента, написать уравнения электродных процессов.
б) Изделие из алюминия склепано с медью. Какой из металлов будет подвергаться коррозии, если эти металлы попадут в кислую среду (НСl)? Составить уравнения происходящих при этом процессов, привести схему образующегося гальванического элемента. Определить продукты коррозии.
№ 12.4. а) Составить схему, написать уравнения токообразующей и электродных реакций для гальванического элемента, у которого один из электродов кобальтовый (СCо 2+ = 10 –1 моль/л), а другой – стандартный водородный. Рассчитать ЭДС элемента при 298 К. Как изменится ЭДС, если концентрация ионов Со 2+ уменьшить в 10 раз? (Ответ: 0,307 В; 0,336 В).
б) Составить уравнения анодного и катодного процессов при коррозии пары магний – свинец в кислой среде и во влажном воздухе. Какие продукты коррозии образуются в первом и во втором случаях?
№ 12.5. а)Каково значение ЭДС элемента, состоящего из медного и свинцового электродов, погруженных в растворы солей этих металлов с концентрациями их ионов 1 моль/л? Изменится или нет ЭДС этого элемента и почему, если концентрации ионов металлов будут составлять 0.001 моль/л? Составить уравнения электродных и токообразующей реакций. Привести схему гальванического элемента. (Ответ: 0,463 В).
б) Привести по одному примеру катодного и анодного покрытия для кобальта. Составить уравнения катодных и анодных процессов во влажном воздухе и в растворе соляной кислоты при нарушении целостности покрытия.
№ 12.6. а) Составить схему, привести уравнения электродных процессов и вычислить ЭДС концентрационного гальванического элемента, состоящего из медных электродов, опущенных в растворы СuSO4 с концентрациями 0,01 и 0,1 моль/л. (Ответ: 0,0295 В).
б)К какому типу покрытий относятся олово на меди и на железе? Какие процессы будут протекать при атмосферной коррозии указанных пар в нейтральной среде? Написатьуравнения катодных и анодных реакций.
№ 12.7. а)После нахождения в растворах каких из приведенных солей масса кадмиевой пластинки увеличится или уменьшится: а) MgCl2; б) Hg(NO3)2;
в) CuSO4; г) AgNO3; д) CaCl2? Ответ обосновать
б) Медное изделие покрыли серебром. К какому типу относится такое покрытие – к анодному или катодному? Составить уравнения электродных процессов коррозии этого изделия при нарушении целостности покрытия во влажном воздухе и в растворе соляной кислоты. Привести схемы образующихся при этом гальванических элементов.
№ 12.8. а) Составить схему, привести уравнения электродных процессов и вычислить ЭДС гальванического элемента, состоящего из свинцовой и магниевой пластин, которые опущены в растворы своих солей с концентрацией ионов Pb 2+ и Mg 2+ , равных 1 моль/л. Изменится ли значение ЭДС, если концентрацию каждого из ионов понизить в 100 раз? Ответ обосновать. (Ответ: 2,237 В).
б) В воду, содержащую растворенный кислород, опустили никелевую пластинку и никелевую пластинку, частично покрытую медью. В каком случае процесс коррозии никеля происходит интенсивнее? Почему? Составить уравнения анодного и катодного процессов для пластинки покрытой медью.
№ 12.9. а)В два сосуда с голубым раствором сульфата меди поместили в первый хромовую пластинку, а во второй платиновую. В каком сосуде цвет раствора постепенно исчезает? Почему? Составить электронные и молекулярные уравнения соответствующих реакций.
б) Какой металл целесообразнее выбрать для протекторной защиты железного изделия: цинк, никель или кобальт? Почему? Составить уравнения анодного и катодного процессов атмосферной коррозии таких изделий. Каков состав продуктов коррозии?
№ 12.10. а) Составить схемы двух гальванических элементов, в одном из которых оловянная пластинка была бы катодом, а в другом анодом. Написать для каждого из этих элементов уравнения электродных (катодных и анодных) процессов и токообразующих реакций.
б) Железо покрыто хромом. Какой из металлов будет корродировать в случае нарушения поверхностного слоя покрытия при атмосферной коррозии? Какое это покрытие катодное или анодное? Составить схему процессов, происходящих на электродах образующегося гальванического элемента.
№ 12.11. а) Составить схему гальванического элемента, в основе работы которого лежит реакция: Ni + Pb(NO3)2 = Ni(NO3)2 + Pb. Написать уравнения электродных (катодных и анодных) процессов. Вычислить ЭДС этого элемента, если СNi 2+ = 0,01 моль/л, а СPb 2+ = 0,0001 моль/л. (Ответ: 0,065 В).
б) Рассчитать энергию Гиббса реакции
и определить, какой из металлов – магний или медь, интенсивнее будет корродировать во влажном воздухе. Стандартные энергии Гиббса образования D¦G 0 Mg(OH)2, Cu(OH)2, H2O (ж) соответственно равны –833,7; –356,9; –237,3 кДж/моль.
№ 12.12. а) Вычислить электродный потенциал цинка в растворе ZnCl2, в котором концентрация Zn 2+ составляет 0,1 моль/л. Как изменится значение потенциала при разбавлении раствора в 100 раз? (Ответ: –0,79 В; –0,85 В).
б) Какой из металлов – алюминий или золото, будет подвергаться коррозии во влажном воздухе по уравнению: 4Ме + 6Н2О (ж) + 3О2 = 4Ме(ОН)3.
Ответ обосновать, рассчитав энергию Гиббса реакции. Стандартные энергии Гиббса образования D¦G 0 Al(OH)3, Au(OH)3, H2O (ж) соответственно равны
–1139,7; –289,9; –237,3 кДж/моль.
№ 12.13. а) Составить схему гальванического элемента, электродами в котором служат пластинки из олова и меди. Исходя из величин стандартных электродных потенциалов, рассчитать значения Е 0 и DG 0 . Определить направление протекания токообразующей реакции. (Ответ: 0,473 В; –91,3 кДж).
б)Какие из перечисленных металлов могут быть использованы для протекторной защиты железного изделия в присутствии электролита, содержащего растворенный кислород в нейтральной среде: алюминий, хром, серебро, кадмий? Привести уравнения анодного и катодного процессов атмосферной коррозии таких изделий. Каков состав продуктов коррозии?
№ 12.14. а) Составить схему гальванического элемента, образованного железом и свинцом, погруженными в растворы их солей с концентрациями ионов металлов 0,01 моль/л. Рассчитать ЭДС. (Ответ: 0,314 В).
б) Изделие из хрома спаяно свинцом. Какой из металлов будет корродировать при попадании такого изделия в кислотную среду (НСl)? Привести уравнения анодного и катодного процессов и образующиеся продукты коррозии.
№ 12.15. а) Исходя из величин стандартных электродных потенциалов, рассчитать значения ЭДС и DG 0 и определить, будет ли работать гальванический элемент, в котором на электродах протекают реакции:
(Ответ: –0,98 В; +189,1 кДж).
б) Составить уравнения анодного и катодного процессов, происходящих при коррозии железа, покрытого серебром, во влажном воздухе и в кислой среде. Определить тип покрытия – анодное или катодное? Какие продукты образуются в результате коррозии?
№ 12.16. а) Исходя из величин стандартных электродных потенциалов, рассчитать значения ЭДС и DG 0 и сделать вывод о возможности протекания реакции в прямом направлении: Cu + 2Ag + 
(Ответ: 0,462 В; –89,2 кДж).
б) Какие металлы могут быть использованы в качестве анодного покрытия сплава Zn – Cd? Привести уравнения анодного и катодного процессов при коррозии такого сплава во влажном воздухе в отсутствие анодного покрытия.
№ 12.17. а) Как изменится масса хромовой пластинки после нахождения в растворах солей: а) CuSO4; б) MgCl2; в) AgNO3; г) CaCl2? Ответ обосновать.
б) Привести уравнения анодного и катодного процессов при коррозии сплава Fe – Sn во влажном воздухе и в кислой среде. Определить продукты коррозии.
№ 12.18. а) Составить схемы двух гальванических элементов, в одном из которых цинк – отрицательный электрод, а в другом – положительный. Привести уравнения токообразующих реакций и электродных процессов.
б) Привести уравнения анодного и катодного процессов, происходящих при коррозии сплава Al – Ni в атмосфере влажного воздуха и в кислой среде (НС1). Определить продукты коррозии.
№ 12.19. а) Электродные потенциалы железа и серебра соответственно равны –0,44 и +0,799 В. Какая реакция самопроизвольно протекает в железо-серебряном гальваническом элементе?
Fe 0 + 2Ag + = Fe 2+ + 2Ag 0 или 2Ag 0 + Fe 2+ = Fe 0 + 2Ag +
Ответ обосновать, рассчитав энергию Гиббса каждой из приведенных реакций.
б) Хромовую пластинку и пластинку из хрома, частично покрытую серебром, поместили в раствор соляной кислоты. В каком случае процесс коррозии хрома протекает более интенсивно? Почему? Привести уравнения соответствующих процессов.
№ 12.20. а) Вычислить ЭДС гальванического элемента, состоящего из водородного электрода, опущенного в чистую воду, и оловянного электрода, опущенного в раствор с концентрацией ионов олова (II) 1 моль/л. (Ответ: 0,16 В).
б) Составить уравнения самопроизвольно протекающих реакций при атмосферной коррозии цинка и олова, находящихся в контакте. Привести схему образующегося гальванического элемента.
Электролиз
Электролиз
Химические реакции, сопровождающиеся переносом электронов (окислительно-восстановительные реакции) делятся на два типа: реакции, протекающие самопроизвольно и реакции, протекающие при прохождении тока через раствор или расплав электролита.
Раствор или расплав электролита помещают в специальную емкость — электролитическую ванну .
Электрический ток — это упорядоченное движение заряженных частиц — ионов, электронов и др. под действием внешнего электрического поля. Электрическое поле в растворе или расплаве электролита создают электроды .
Электроды — это, как правило, стержни из материала, проводящего электрический ток. Их помещают в раствор или расплав электролита, и подключают к электрической цепи с источником питания.
При этом отрицательно заряженный электрод катод — притягивает положительно заряженные ионы — катионы . Положительно заряженный электрод ( анод ) притягивает отрицательно заряженные частицы ( анионы ). Катод выступает в качестве восстановителя, а анод — в качестве окислителя.
Различают электролиз с активными и инертными электродами. Активные (растворимые) электроды подвергаются химическим превращениям в процессе электролиза. Обычно их изготавливают из меди, никеля и других металлов. Инертные (нерастворимые) электроды химическим превращениям не подвергаются. Их изготавливают из неактивных металлов, например, платины , или графита .
Электролиз растворов
Различают электролиз раствора или расплава химического вещества. В растворе присутствует дополнительное химическое вещество — вода, которая может принимать участие в окислительно-восстановительных реакциях.
Катодные процессы
В растворе солей катод притягивает катионы металлов. Катионы металлов могут выступать в качестве окислителей. Окислительные способности ионов металлов различаются. Для оценки окислительно-восстановительных способностей металлов применяют электро-химический ряд напряжений :
Каждый металл характеризуется значением электрохимического потен-циала. Чем меньше потенциал , тем больше восстановительные свойства металла и тем меньше окислительные свойства соответствующего иона этого металла. Разным ионам соответствуют разные значения этого потенциала. Электрохимический потенциал — относительная величина. Электрохимический потенциал водорода принят равным нулю.
Также около катода находятся молекулы воды Н2О. В составе воды есть окислитель — ион H + .
При электролизе растворов солей на катоде наблюдаются следующие закономерности:
1. Если металл в соли — активный ( до Al 3+ включительно в ряду напряжений ), то вместо металла на катоде восстанавливается (разряжается) водород , т.к. потенциал водорода намного больше. Протекает процесс восстановления молекулярного водорода из воды, при этом образуются ионы OH — , среда возле катода — щелочная:
2H2O +2ē → H2 + 2OH —
Например , при электролизе раствора хлорида натрия на катоде будет вос-станавливаться только водород из воды.
2. Если металл в соли – средней активности (между Al 3+ и Н + ) , то на катоде восстанавливается (разряжается) и металл , и водород , так как потенциал таких металлов сравним с потенциалом водорода:
Me n+ + nē → Me 0
2 H + 2O +2ē → H2 0 + 2OH —
Например , при электролизе раствора сульфата железа (II) на катоде будет восстанавливаться (разряжаться) и железо, и водород:
Fe 2+ + 2ē → Fe 0
2 H + 2O +2ē → H2 0 + 2OH —
3. Если металл в соли — неактивный (после водорода в ряду стандартных электрохимических металлов) , то ион такого металла является более сильным окислителем, чем ион водорода, и на катоде восстанавливается только металл:
Me n+ + nē → Me 0
Например, при электролизе раствора сульфата меди (II) на катоде будет восстанавливаться медь:
Cu 2+ + 2ē → Cu 0
4. Если на катод попадают катионы водорода H + , то они и восстанавливаются до молекулярного водорода:
2H + + 2ē → H2 0
Анодные процессы
Положительно заряженный анод притягивает анионы и молекулы воды. Анод – окислитель. В качестве восстановителей выступаю либо анионы кислотных остаток, либо молекулы воды (за счет кислорода в степени окисления -2: H 2 O -2 ).
При электролизе растворов солей на аноде наблюдаются следующие закономерности:
1. Если на анод попадает бескислородный кислотный остаток , то он окисляется до свободного состояния (до степени окисления 0):
неМе n- – nē = неМе 0
Например : при электролизе раствора хлорида натрия на аноде окисляют-ся хлорид-ионы:
2Cl — – 2ē = Cl2 0
Действительно, если вспомнить Периодический закон: при увеличении электроотрицательности неметалла его восстановительные свойства уменьшаются. А кислород – второй по величине электроотрицательности элемент. Таким образом, проще окислить практически любой неметалл, а не кислород. Правда, есть одно исключение . Наверное, вы уже догадались. Конечно же, это фтор. Ведь электроотрицательность фтора больше, чем у кислорода. Таким образом, при электролизе растворов фторидов окисляться будут именно молекулы воды, а не фторид-ионы :
2H2 O -2 – 4ē → O2 0 + 4H +
2. Если на анод попадает кислородсодержащий кислотный остаток, либо фторид-ион , то окислению подвергается вода с выделением молекулярно-го кислорода:
2H2 O -2 – 4ē → O2 0 + 4H +
3. Если на анод попадает гидроксид-ион, то он окисляется и происходит выделение молекулярного кислорода:
4 O -2 H – – 4ē → O2 0 + 2H2O
4. При электролизе растворов солей карбоновых кислот окислению под-вергается атом углерода карбоксильной группы, выделяется углекислый газ и соответствующий алкан.
Например , при электролизе растворов ацетатов выделяется углекислый газ и этан:
2 CH3 C +3 OO – –2ē → 2 C +4 O2+ CH3-CH3
Суммарные процессы электролиза
Рассмотрим электролиз растворов различных солей.
Например , электролиз раствора сульфата меди. На катоде восстанавливаются ионы меди:
Катод (–): Cu 2+ + 2ē → Cu 0
На аноде окисляются молекулы воды:
Анод (+): 2H2 O -2 – 4ē → O2 + 4H +
Сульфат-ионы в процессе не участвуют. Мы их запишем в итоговом уравнении с ионами водорода в виде серной кислоты:
2 Cu 2+ SO4 + 2H2 O -2 → 2 Cu 0 + 2H2SO4 + O2 0
Электролиз раствора хлорида натрия выглядит так:
На катоде восстанавливается водород:
Катод (–): 2 H + 2O +2ē → H2 0 + 2OH –
На аноде окисляются хлорид-ионы:
Анод (+): 2 Cl – – 2ē → Cl2 0
Ионы натрия в процессе электролиза не участвуют. Мы записываем их с гидроксид-анионами в суммарном уравнении электролиза раствора хлорида натрия :
2 H + 2O +2Na Cl – → H2 0 + 2NaOH + Cl2 0
Следующий пример : электролиз водного раствора карбоната калия.
На катоде восстанавливается водород из воды:
Катод (–): 2 H + 2O +2ē → H2 0 + 2OH –
На аноде окисляются молекулы воды до молекулярного кислорода:
Анод (+): 2H2 O -2 – 4ē → O2 0 + 4H +
Таким образом, при электролизе раствора карбоната калия ионы калия и карбонат-ионы в процессе не участвуют. Происходит электролиз воды:
2 H2 + O -2 → 2 H2 0 + O2 0
Еще один пример : электролиз водного раствора хлорида меди (II).
На катоде восстанавливается медь:
Катод (–): Cu 2+ + 2ē → Cu 0
На аноде окисляются хлорид-ионы до молекулярного хлора:
Анод (+): 2 Cl – – 2ē → Cl2 0
Таким образом, при электролизе раствора карбоната калия происходит электролиз воды:
Cu 2+ Cl2 – → Cu 0 + Cl2 0
Еще несколько примеров: электролиз раствора гидроксида натрия.
На катоде восстанавливается водород из воды:
Катод (–): 2 H + 2O +2ē → H2 0 + 2OH –
На аноде окисляются гидроксид-ионы до молекулярного кислорода:
Анод (+): 4 O -2 H – – 4ē → O2 0 + 2H2O
Таким образом, при электролизе раствора гидроксида натрия происходит разложение воды, катионы натрия в процессе не участвуют:
2 H2 + O -2 → 2 H2 0 + O2 0
Электролиз расплавов
При электролизе расплава на аноде окисляются анионы кислотных остатков, а на катоде восстанавливаются катионы металлов. Молекул воды в системе нет.
Например: электролиз расплава хлорида натрия. На катоде восстанавли-ваются катионы натрия:
Катод (–): Na + + ē → Na 0
На аноде окисляются анионы хлора:
Анод (+): 2 Cl – – 2ē → Cl2 0
Суммарное уравнение электролиза расплава хлорида натрия:
2 Na + Cl – → 2 Na 0 + Cl2 0
Еще один пример: электролиз расплава гидроксида натрия. На катоде восстанавливаются катионы натрия:
Катод (–): Na + + ē → Na 0
На аноде окисляются гидроксид-ионы:
Анод (+): 4 OH – – 4ē → O2 0 + 2H2O
Суммарное уравнение электролиза расплава гидроксида натрия:
4 Na + OH – → 4 Na 0 + O2 0 + 2H2O
Многие металлы получают в промышленности электролизом расплавов.
Например , алюминий получают электролизом раствора оксида алюминия в расплаве криолита. Криолит – Na3[AlF6] плавится при более низкой температуре (1100 о С), чем оксид алюминия (2050 о С). А оксид алюминия отлично растворяется в расплавленном криолите.
В растворе криолите оксид алюминия диссоциирует на ионы:
На катоде восстанавливаются катионы алюминия:
Катод (–): Al 3+ + 3ē → Al 0
На аноде окисляются алюминат-ионы:
Анод (+): 4Al O 3 3 – – 12ē → 2Al2O3 + 3 O2 0
Общее уравнение электролиза раствора оксида алюминия в расплаве криолита:
2 Al 2 О 3 = 4 Al 0 + 3 О 2 0
В промышленности при электролизе оксида алюминия в качестве электродов используют графитовые стержни. При этом электроды частично окисляются (сгорают) в выделяющемся кислороде:
C 0 + О2 0 = C +4 O2 -2
Электролиз с растворимыми электродами
Если материал электродов выполнен из того же металла, который присут-ствует в растворе в виде соли, или из более активного металла, то на аноде разряжаются не молекулы воды или анионы, а окисляются частицы самого металла в составе электрода.
Например , рассмотрим электролиз раствора сульфата меди (II) с медными электродами.
На катоде разряжаются ионы меди из раствора:
Катод (–): Cu 2+ + 2ē → Cu 0
На аноде окисляются частицы меди из электрода :
Анод (+): Cu 0 – 2ē → Cu 2+



