Электролиз по Кольбе – это электролиз растворов солей карбоновых кислот. В ходе реакции образуются соответствующие алканы.
Например, рассмотрим электролиз водного раствора ацетата натрия CH3COONa. В водном растворе ацетат натрия практически полностью диссоциирует:
CH3COONa → CH3COO – + Na +
При этом на катод притягиваются катионы натрия Na + и молекулы воды H2O. Восстанавливаться на катоде будут молекулы воды, т.к. окислительные свойства ионов водорода превышают окислительные свойства катионов щелочных металлов:
K(-): 2H2O + 2e = H2 + 2OH –
На аноде окисляются ацетат-ионы, а именно, атом углерода карбоксильной группы. При этом от карбоксильной группы остаются метильные радикалы, которые образуют газообразный этан.
A(+): 2CH3COO – — 2e = 2CO2 + CH3–CH3
Суммарное уравнение электролиза водного раствора ацетата натрия:
В общем виде получается:
2R–COONa + 2H2O → H2 + 2NaOH + 2CO2 + R–R
То есть при электролизе раствора пропионата натрия образуется бутан:
Электролиз
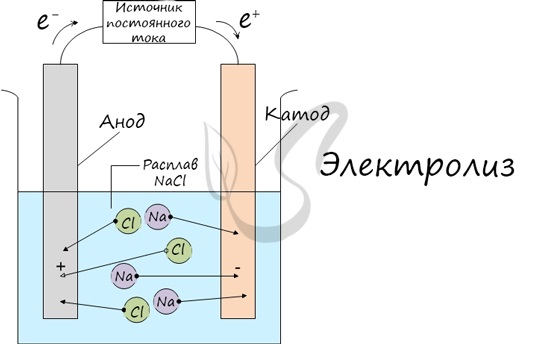
Электролиз (греч. elektron — янтарь + lysis — разложение) — химическая реакция, происходящая при прохождении постоянного тока через электролит. Это разложение веществ на их составные части под действием электрического тока.
Процесс электролиза заключается в перемещении катионов (положительно заряженных ионов) к катоду (заряжен отрицательно), и отрицательно заряженных ионов (анионов) к аноду (заряжен положительно).
Итак, анионы и катионы устремляются соответственно к аноду и катоду. Здесь и происходит химическая реакция. Чтобы успешно решать задания по этой теме и писать реакции, необходимо разделять процессы на катоде и аноде. Именно так и будет построена эта статья.
Катод
К катоду притягиваются катионы — положительно заряженные ионы: Na + , K + , Cu 2+ , Fe 3+ , Ag + и т.д.
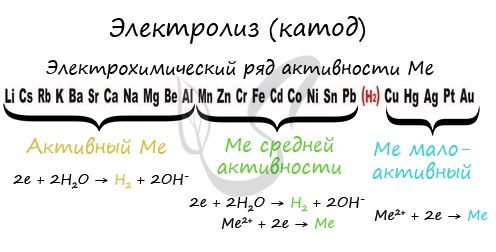
Чтобы установить, какая реакция идет на катоде, прежде всего, нужно определиться с активностью металла: его положением в электрохимическом ряду напряжений металлов.
Если на катоде появился активный металл (Li, Na, K) то вместо него восстанавливаются молекулы воды, из которых выделяется водород. Если металл средней активности (Cr, Fe, Cd) — на катоде выделяется и водород, и сам металл. Малоактивные металлы выделяются на катоде в чистом виде (Cu, Ag).
Замечу, что границей между металлами активными и средней активности в ряду напряжений считается алюминий. При электролизе на катоде металлы до алюминия (включительно!) не восстанавливаются, вместо них восстанавливаются молекулы воды — выделяется водород.
В случае, если на катод поступают ионы водорода — H + (например при электролизе кислот HCl, H2SO4) восстанавливается водород из молекул кислоты: 2H + — 2e = H2
К аноду притягиваются анионы — отрицательно заряженные ионы: SO4 2- , PO4 3- , Cl — , Br — , I — , F — , S 2- , CH3COO — .
При электролизе кислородсодержащих анионов: SO4 2- , PO4 3- — на аноде окисляются не анионы, а молекулы воды, из которых выделяется кислород.
Бескислородные анионы окисляются и выделяют соответствующие галогены. Сульфид-ион при оксилении окислении серу. Исключением является фтор — если он попадает анод, то разряжается молекула воды и выделяется кислород. Фтор — самый электроотрицательный элемент, поэтому и является исключением.
Анионы органических кислот окисляются особым образом: радикал, примыкающий к карбоксильной группе, удваивается, а сама карбоксильная группа (COO) превращается в углекислый газ — CO2.
Примеры решения
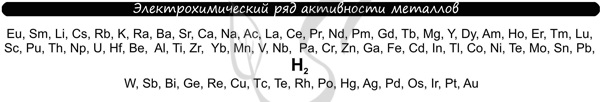
В процессе тренировки вам могут попадаться металлы, которые пропущены в ряду активности. На этапе обучения вы можете пользоваться расширенным рядом активности металлов.
Теперь вы точно будете знать, что выделяется на катоде 😉
Итак, потренируемся. Выясним, что образуется на катоде и аноде при электролизе растворов AgCl, Cu(NO3)2, AlBr3, NaF, FeI2, CH3COOLi.
Иногда в заданиях требуется записать реакцию электролиза. Сообщаю: если вы понимаете, что образуется на катоде, а что на аноде, то написать реакцию не составляет никакого труда. Возьмем, например, электролиз NaCl и запишем реакцию:
NaCl + H2O → H2 + Cl2 + NaOH (обычно в продуктах оставляют именно запись «NaOH», не подвергая его дальнейшему электролизу)
Натрий — активный металл, поэтому на катоде выделяется водород. Анион не содержит кислорода, выделяется галоген — хлор. Мы пишем уравнение, так что не можем заставить натрий испариться бесследно 🙂 Натрий вступает в реакцию с водой, образуется NaOH.
Запишем реакцию электролиза для CuSO4:
Медь относится к малоактивным металлам, поэтому сама в чистом виде выделяется на катоде. Анион кислородсодержащий, поэтому в реакции выделяется кислород. Сульфат-ион никуда не исчезает, он соединяется с водородом воды и превращается в серую кислоту.
Электролиз расплавов
Все, что мы обсуждали до этого момента, касалось электролиза растворов, где растворителем является вода.
Перед промышленной химией стоит важная задача — получить металлы (вещества) в чистом виде. Малоактивные металлы (Ag, Cu) можно легко получать методом электролиза растворов.
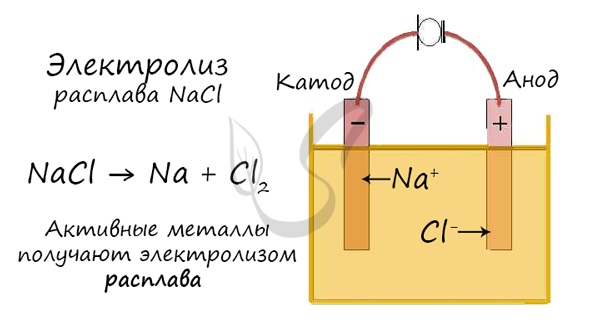
Но как быть с активными металлами: Na, K, Li? Ведь при электролизе их растворов они не выделяются на катоде в чистом виде, вместо них восстанавливаются молекулы воды и выделяется водород. Тут нам как раз пригодятся расплавы, которые не содержат воды.
В безводных расплавах реакции записываются еще проще: вещества распадаются на составные части:
© Беллевич Юрий Сергеевич 2018-2022
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Способ получения пероксимуравьиной кислоты и ее солей
Владельцы патента RU 2299878:
Настоящее изобретение относится к способу получения пероксимуравьиной кислоты и ее солей. Сущность предложенного способа заключается в том, что проводят электролиз 0,5-2,0 М водного раствора муравьиной кислоты или ее солей щелочных металлов в диафрагменном электролизере на диоксидно-свинцовом аноде при плотностях тока 0,05-0,5 А/см 2 в присутствии роданида аммония при его концентрации 1,0-1,5 г/л. Технический результат — исключение использования сильных взрывоопасных окислителей, высокая селективность процесса синтеза, возможность непрерывного осуществления процесса и получение конечного продукта высокой чистоты. 4 табл.
Изобретение относится к области технологии получения органических перекисных соединений, которые могут быть использованы для отбеливания целлюлозы, крахмала, очистки масел, как антисептик в медицине, в сельском хозяйстве, как инициатор в реакциях полимеризации и конденсации, в органическом синтезе при гидроксилировании жирных кислот и олефинов, а также в производстве окиси пропилена, глицидола и других эпоксисоединений (реакция Прилежаева).
Известен способ получения надмуравьиной кислоты из муравьиной кислоты с использованием концентрированных растворов перекиси водорода (в чистом виде муравьиная кислота не получена) [1].
Сущность препаративного синтеза надмуравьиной кислоты химическим методом заключается в том, что стехиометрическую смесь 85%-ной кислоты и 90%-ной перекиси водорода сливают в стеклянную колбу (вначале вливают перекись водорода, а затем муравьиную кислоту), встряхивают и оставляют на 12-16 часов при температуре не выше 10°С. Повышения концентрации надмуравьиной кислоты добиваются декантацией полученного раствора при низких температурах.
Недостаток химического способа получения растворов надмуравьиной кислоты в том, что:
— синтез протекает в несколько стадий;
— используются агрессивные окислители;
— применяется сложное технологическое оборудование для предотвращения взрывов и для поддержания низких температур.
Наиболее близким по технической сущности способом получения пероксимуравьиной кислоты является способ получения пероксиуксусной кислоты [2], сущность которого состоит в том, что проводят электролиз водных растворов ацетата щелочного металла или аммония в анодном отделении диафрагменного электролизера в присутствии 0,5-2,0 г/л добавки роданида щелочного металла или аммония при плотности тока 0,05-1,0 А/см 2 с последующим концентрированном образующегося водного раствора пероксикислоты выпариванием или вакуумной перегонкой.
Недостатком синтеза пероксиуксусной кислоты является ее электрохимическое получение из водных растворов солей уксусной кислоты в диафрагменном электролизере с использованием катионитовой мембраны при длительном электролизе. Электросинтез надуксусной кислоты непосредственно из уксусной не представляется возможным ввиду незначительной электропроводности последней.
Задачей настоящего изобретения является разработка способа электрохимического синтеза пероксимуравьиной кислоты и ее солей электролизом водных растворов муравьиной кислоты и ее солей щелочных металлов.
Техническим результатом данного изобретения являются селективность процесса синтеза и получение высокой чистоты конечных продуктов — пероксимуравьиной кислоты и ее солей. Электрохимический метод синтеза в отличие от химического протекает в одну стадию и может осуществляться непрерывно.
Сущностью предложенного способа получения пероксимуравьиной кислоты и ее солей является то, что проводят электролиз 0,5-2,0М водного раствора муравьиной кислоты и ее солей щелочных металлов в диафрагменном электролизере на диоксидно-свинцовом аноде при плотностях тока 0,05-0,5 А/см 2 в присутствии роданида аммония при его концентрации 1,0-1,5 г/л.
Предложенный метод синтеза заключается в том, что надмуравьиную кислоту получают как из водных растворов формиатов, так и непосредственно из муравьиной кислоты, т.к. последняя обладает достаточной электропроводностью для проведения электролиза при небольших напряжениях на электролизере (следует отметить, что электросинтез надуксусной кислоты осуществляют только из водных растворов ее солей [2]). Пероксиформиаты щелочных металлов можно синтезировать из водных растворов соответствующих формиатов.
Электролиз муравьиной кислоты и ее солей также как электролиз и других карбоновых кислот и их солей протекает по реакции синтеза Кольбе.
Однако в отличие от всех остальных карбоновых кислот (в том числе и угольная) и их солей в молекуле муравьиной кислоты и ее солей имеется водородный радикал. Это отличие и приводит к тому, что реакция синтеза Кольбе протекает по следующей схеме:
Как известно из литературы [3], НСООН на электродах из платиновых металлов еще при низких анодных потенциалах подвергается каталитическому распаду. Чтобы исключить каталитический распад, необходимо использовать диоксидно-свинцовый электрод. На аноде из диоксида свинца в присутствии известных ингибирующих кислородную реакцию добавок (F — , Cl — , SCN — ) реакция Кольбе в растворах муравьиной кислоты или ее солей протекает с участием молекул воды по следующей схеме:
с образованием пероксиформиат-ионов.
Однако электролизу водных растворов муравьиной кислоты и ее солей должно предшествовать модифицирование диоксидно-свинцового анода при низких потенциалах в присутствии поверхностно-активных добавок (CSN — , F — , Cl — ). На аноде с модифицированной поверхностью потенциал разряда молекул воды и выделения кислорода смещается в область высоких анодных потенциалов, где происходит окисление формиат-ионов до пероксиформиат-ионов по уравнению реакции (2).
В анодное отделение электролизера с катионитовой мембраной, разделяющей анодную и катодную части, заливают 60 мл водного раствора роданистого аммония из расчета 1,0 г/л. Анодом служит диоксидно-свинцовый электрод с геометрической поверхностью 4 см 2 . В катодное отделение заливают столько же по объему 0,1М раствора серной или соляной кислоты. В качестве материала катода использовали платину (Sгеом.=5 см 2 ) или пирографит с поверхностью 20 см 2 . После предварительной поляризации анода в исходном растворе плотностью тока 0,01 мА/см 2 к анолиту добавляют 3,2 мл 86%-ного водного раствора муравьиной кислоты. Затем плотность тока повышают до 0,05 А/см 2 и электролиз ведут в течение 3-х часов. Температура анолита в процессе электросинтеза поддерживается в пределах 10-20°С. При более высоких температурах выход конечного продукта падает из-за его постепенного разложения. Результаты электросинтеза надмуравьиной кислоты в зависимости от исходной концентрации НСООН представлены в табл.1.
Данные электросинтеза надмуравьиной кислоты в растворах муравьиной кислоты в зависимости от плотности тока и концентрации роданида аммония приведены в табл.3 и 4 соответственно.
Концентрирование полученных растворов пероксимуравьиной кислоты проводится выше описанным методом, как и в случае химического получения пероксимуравьиной кислоты.
Идентификацию конечного продукта осуществляли следующими качественными реакциями на перекисную группу:
1. Полученный раствор НСОООН взбалтывают, подкисляя несколькими каплями разбавленной серной кислоты с этиловым эфиром и несколькими каплями раствора бихромата калия; при этом эфирный слой окрашивается в темно-синий цвет от надхромовой кислоты, образовавшейся под влиянием пероксимуравьиной кислоты, растворившейся в эфире и придавшей ему указанную окраску. Хотя соли хромовых кислот являются окислителями, но при действии перекисей они способны окисляться в еще более богатую кислородом надхромовую кислоту Н2Cr2О8 по схеме:
Данная реакция позволяет обнаружить перекисное соединение при концентрации 0,001%.
2. Реакция с йодистым калием в присутствии винной кислоты. К 2 мл 5%-ной винной кислоты добавляют 2 капли 5%-ного раствора FeSO4 и (NH4)2SO4. После смешения с раствором пероксимуравьиной кислоты добавляют 5-6 капель едкого натра; при этом появляется фиолетовое окрашивание. Сульфат железа добавляют для ускорения реакции [4].
При идентификации пероксимуравьиной кислоты также применялся метод ИК — спектроскопии. Для сравнительного исследования были синтезированы соли натрия пероксимуравьиной кислоты химическим и электрохимическим методами. Установлено, что в спектре пероксиформиата натрия полосы поглощения, связанные с -O-O- группой, проявляются в области 1550-1450 см -1 (широкая полоса), и отчетливые полосы в областях 2760 см -1 и 2830 см -1 , которые отсутствуют в спектрах формиата натрия. Спектрометрическое определение проводили на спектрометре Infralum — FT-801 в диапазоне волн 500-4000 см -1 . Аподизация — треугольная, частота — 8 скан/сек. Образцы для снятия спектров готовились растиранием продуктов электролиза — солей пероксимуравьиной кислоты с бромистым калием и прессованием в микротаблетки в пресс-форме. Химически пероксиформиат натрия получали из пероксимуравьиной кислоты, синтезируемой методом, описанным в [1].
Количественное определение содержания активного кислорода в полученной пероксимуравьиной кислоте определяли методом йодометрического титрования.
Метод йодометрии основан на реакции:
Выделившийся йод оттитровывали 0,1н. раствором тиосульфата натрия. Индикатором служит раствор крахмала, дающий с йодом характерное синее окрашивание. Исследуемые растворы также сравнивали с приготовленными стандартными растворами на сходимость результатов, определяемых вышеописанным методом.
В анодное отделение электролизера с анионитовой мембраной, разделяющей анодную и катодную части, заливают 60 мл водного раствора роданистого аммония из расчета 1,3 г/л. В качестве анода использовали диоксидно-свинцовый электрод с поверхностью 4 см 2 . В катодное отделение заливают столько же по объему 0,1М раствора гидроксида натрия или калия. Катодом служит пластина из нержавеющей стали поверхностью 20 см 2 . После предварительной поляризации анода в растворе роданида аммония в течение 15-20 мин в анолите растворяли 4,08 г формиата натрия для получения 1,0 М раствора. Электролиз ведут при плотности тока 0,05 А/см 2 в течение 3-х часов. Температура анолита в процессе электросинтеза поддерживается в пределах 10-20°С. Установлено, что повышение температуры на электролизере отрицательно влияет на выход конечного продукта.
Как видно из табл.1 и 2, в растворах муравьиной кислоты и формиатов щелочных металлов с повышением концентрации исходного электролита более 2,0 М выход по току уменьшается.
Проводится аналогично примеру 2. Электролизу подвергались растворы солей муравьиной кислоты при различных значениях плотности тока. Результаты электролиза представлены в табл.3, по которым видно, что максимальные выходы по веществу и по току получаются при плотностях анодного тока 0,05-0,5 А/см 2 .
Проводится аналогично примеру 2. Электролизу подвергаются растворы НСООН и ее солей при различных концентрациях роданида аммония. Без добавки CSN — -ионов выход пероксимуравьиной кислоты и ее солей незначителен (табл.1 и 2). Из результатов опытов, представленных в табл.4, видно, что максимальные выходы по веществу и по току надмуравьиной кислоты с концентрациями добавки роданида аммония лежат в пределах 1,0-1,5 г/л, а для солей надмуравьиной кислоты — 0,5-2 г/л. При концентрациях NH4SCN>2 г/л выход по току падает и конечный продукт загрязняется роданидсодержащими соединениями.
Синтезируемые в водных растворах пероксимуравьиная кислота и ее соли по физическим и химическим свойствам идентичны соответствующим соединениям, получаемым известными химическими методами.
Приведенный метод электросинтеза пероксимуравьиной кислоты и ее солей перед традиционными химическими методами синтеза пероксимуравьиной кислоты имеет ряд преимуществ:
— исключает использование сильных окислителей (пероксид водорода, перманганат калия, надсерная кислота и т.д.);
— обладает селективностью для данного процесса синтеза и может регулироваться поддержанием тока или потенциала;
— осуществить процесс непрерывно;
— получение конечного продукта высокой чистоты, с которым и связано замедление его распада при комнатной температуре;
исключает взрывоопасность процесса синтеза; возможность автоматического контроля процесса синтеза.
| НСООН С, моль/л | NH4SCN С, г/л | i. А/см 2 | Q, А-ч | Выход | |
| По веществу, % | По току, % | ||||
| 0,2 | 0 | 0.1 | 1 | — | 23 |
| 0,2 | 1 | 0.1 | 1 | 40 | 52 |
| 0,5 | 1 | 0.1 | 2 | 47 | 56 |
| 1,0 | 1 | 0.1 | 3 | 60 | 70 |
| 1,5 | 1 | 0.1 | 4 | 58 | 72 |
| 2,0 | 1 | 0.1 | 5 | 49 | 65 |
| 2,5 | 1 | 0.1 | 5 | 35 | 48 |
| NaHCOO С, моль/л | NH4SCN С, г/л | i, А/см 2 | Q, А-ч | Выход | |
| По веществу, % | По току, % | ||||
| 0,2 | 0 | 0.1 | 1 | 10 | 22 |
| 0,2 | 1 | 0.1 | 1 | 67 | 70 |
| 0,5 | 1 | 0.1 | 2 | 70 | 75 |
| 1,0 | 1 | 0.1 | 3 | 78 | 81 |
| 1,5 | 1 | 0.1 | 4 | 80 | 85 |
| 2,0 | 1 | 0.1 | 5 | 75 | 81 |
| 2,5 | 1 | 0.1 | 5 | 42 | 51 |
| С, моль/л | NH4SCN С, г/л | i, А/см 2 | Q, А-ч | Выход | |
| По веществу, % | По току, % | ||||
| 1,0 NaHCOO | 1 | 0,005 | 3 | 27 | 31 |
| 1,0 NaHCOO | 1 | 0,01 | 3 | 46 | 55 |
| 1,0 КНСОО | 1 | 0,05 | 3 | 56 | 68 |
| 1,0 NaHCOO | 1 | 0,1 | 3 | 82 | 90 |
| 1,0 НСООН | 1 | 0,1 | 3 | 60 | 70 |
| 1,0 КНСОО | 1 | 0,25 | 3 | 76 | 80 |
| 1,0 КНСОО | 1 | 0,5 | 3 | 70 | 75 |
| 1,0 НСООН | 1 | 0,5 | 3 | 50 | 52 |
| 1,0 КНСОО | 1 | 0,8 | 3 | 52 | 60 |
| С, моль/л | NH4SCN С, г/л | i, А/см 2 | Q, A-ч | Выход | |
| По веществу, % | По току, % | ||||
| 1,0 NaHCOO | 0,5 | 0,1 | 2 | 28 | 36 |
| 1,0 НСООН | 0,5 | 0,1 | 2 | 13 | 20 |
| 1,0 NaHCOO | 0,1 | 0,1 | 2 | — | 32 |
| 1,0 КНСОО | 1,0 | 0,1 | 2 | 76 | 90 |
| 1,0 НСООН | 1,5 | 0,1 | 2 | 55 | 63 |
| 1,0 КНСОО | 1,5 | 0,1 | 2 | 65 | 75 |
| 1,0 NaHCOO | 2,0 | 0,1 | 2 | 35 | 41 |
| 1,0 НСООН | 2,0 | 0,1 | 2 | 16 | 23 |
1. Антоновский В.Л. Органические перекисные инициаторы. М., 1972, 341-361; Swern D., в кн. Organic peroxides, v.1, N.Y.-[a,o], 1970, p.313-474.
2. Патент РФ № 2216537, от 28.06.2002, бюл. № 32, 20.11.2003.
3. Смолин А.В., Подловченко Б.И., Максимов Ю.М. Электроокисление муравьиной кислоты в сернокислом электролите на электролитических осадках палладия. //Электрохимия. 1997. Т.33. № 4, с.477-484.
4. Перекись водорода и перекисные соединения. Под ред. проф. М.Е.Позина. ГНТИ ХЛ, М., 1951, с.482.
Способ получения пероксимуравьиной кислоты и ее солей, отличающийся тем, что проводят электролиз 0,5-2,0 М водного раствора муравьиной кислоты или ее солей щелочных металлов в диафрагменном электролизере на диоксидно-свинцовом аноде при плотностях тока 0,05-0,5 А/см 2 в присутствии роданида аммония при его концентрации 1,0-1,5 г/л.