Электролитической диссоциацией называют процесс, в ходе которого молекулы растворенного вещества распадаются на ионы в результате взаимодействия с растворителем (воды). Диссоциация является обратимым процессом.
Диссоциация обуславливает ионную проводимость растворов электролитов. Чем больше молекул вещества распадается на ионы, тем лучше оно проводит электрический ток и является более сильным электролитом.
В общем виде процесс электролитической диссоциации можно представить так:
KA ⇄ K + (катион) + A — (анион)
Замечу, что сила кислоты определяется способностью отщеплять протон. Чем легче кислота его отщепляет, тем она сильнее.
У HF крайне затруднен процесс диссоциации из-за образования водородных связей между F (самым электроотрицательным элементом) одной молекулы и H другой молекулы.
- Электролитическая диссоциация
- Степень диссоциации
- Классификация электролитов
- Диссоциация электролитов
- Константа диссоциации
- Примеры решения задач
- Задачи для самостоятельного решения
- Электролитическая диссоциация: решение задач
- Диссоциация кислот и оснований
- Диссоциация малорастворимых веществ
- Примеры решения задач
Ступени диссоциации
Некоторые вещества диссоциируют на ионы не в одну стадию (как NaCl), а ступенчато. Это характерно для многоосновных кислот: H2SO4, H3PO4.
Посмотрите на ступенчатую диссоциацию ортофосфорной кислоты:
Важно заметить, что концентрация ионов на разных ступенях разная. На первых ступенях ионов всегда много, а до последних доходят не все молекулы. Поэтому в растворе ортофосфорной кислоты концентрация дигидрофосфат-анионов будет больше, чем фосфат-анионов.
Для серной кислоты диссоциация будет выглядеть так:
Для средних солей диссоциация чаще всего происходит в одну ступень:
Из одной молекулы ортофосфата натрия образовалось 4 иона.
Из одной молекулы сульфата калия образовалось 3 иона.
Электролиты и неэлектролиты
Химические вещества отличаются друг от друга по способности проводить электрический ток. Исходя из этой способности, вещества делятся на электролиты и неэлектролиты.
Электролиты — жидкие или твердые вещества, в которых присутствуют ионы, способные перемещаться и проводить электрический ток. Связи в их молекулах обычно ионные или ковалентные сильнополярные.
К ним относятся соли, сильные кислоты и щелочи (растворимые основания).
Степень диссоциации сильных электролитов составляет от 0,3 до 1, что означает 30-100% распад молекул, попавших в раствор, на ионы.
Неэлектролиты — вещества недиссоциирующие в растворах на ионы. В молекулах эти веществ связи ковалентные неполярные или слабополярные.
К неэлектролитам относятся многие органические вещества, слабые кислоты, нерастворимые в воде основания и гидроксид аммония.
Степень их диссоциации до 0 до 0.3, то есть в растворе неэлектролита на ионы распадается до 30% молекул. Они плохо или вообще не проводят электрический ток.
Молекулярное, полное и сокращенное ионные уравнения
Молекулярное уравнение представляет собой запись реакции с использованием молекул. Это те уравнения, к которым мы привыкли и которыми наиболее часто пользуемся. Примеры молекулярных уравнений:
Полные ионные уравнения записываются путем разложения молекул на ионы. Запомните, что нельзя раскладывать на ионы:
- Слабые электролиты (в их числе вода)
- Осадки
- Газы
Сокращенное ионное уравнение записывается путем сокращения одинаковых ионов из левой и правой части. Просто, как в математике — остается только то, что сократить нельзя.
© Беллевич Юрий Сергеевич 2018-2022
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Блиц-опрос по теме Электролитическая диссоциация
Электролитическая диссоциация
Материалы портала onx.distant.ru
Примеры решения задач
Задачи для самостоятельного решения
Степень диссоциации
Вещества, которые в растворах или расплавах полностью или частично распадаются на ионы, называются электролитами.
Степень диссоциации α — это отношение числа молекул, распавшихся на ионы N′ к общему числу растворенных молекул N:
α = N′/N
Степень диссоциации выражают в процентах или в долях единицы. Если α =0, то диссоциация отсутствует и вещество не является электролитом. В случае если α =1, то электролит полностью распадается на ионы.
Классификация электролитов
Согласно современным представлениям теории растворов все электролиты делятся на два класса: ассоциированные (слабые) и неассоциированные (сильные) . Неассоциированные электролиты в разбавленных растворах практически полностью диссоциированы на ионы. Для этого класса электролитов a близко к единице (к 100 %). Неассоциированными электролитами являются, например, HCl, NaOH, K2SO4 в разбавленных водных растворах.
Ассоциированные электролиты подразделяются на три типа:
- Слабые электролиты существуют в растворах как в виде ионов, так и в виде недиссоциированных молекул. Примерами ассоциированных электролитов этой группы являются, в частности, Н2S, Н2SO3, СН3СOОН в водных растворах.
- Ионные ассоциаты образуются в растворах путем ассоциации простых ионов за счет электростатического взаимодействия. Ионные ассоциаты возникают в концентрированных растворах хорошо растворимых электролитов. В результате в растворе находятся как простые ионы, так и ионные ассоциаты. Например, в концентрированном водном растворе КCl образуются простые ионы К + , Cl — , а также возможно образование ионных пар (К + Cl — ), ионных тройников (K2Cl + , KCl2 — ) и ионных квадруполей (K2Cl2, KCl3 2- , K3Cl 2+ ).
- Комплексные соединения (как ионные, так и молекулярные), внутренняя сфера которых ступенчато диссоциирует на ионные и (или) молекулярные частицы.
Примеры комплексных ионов: [Cu(NH3)4] 2+ , [Fe(CN)6] 3+ , [Cr(H2O)3Cl2] + .
При таком подходе один и тот же электролит может относиться к различным типам в зависимости от концентрации раствора, вида растворителя и температуры. Подтверждением этому являются данные, приведенные в таблице.
Таблица. Характеристика растворов KI в различных растворителях
| Концентрация электролита, С, моль/л | Температура t, о С | Растворитель | Тип электролита |
| 0,01 | 25 | Н2О | Неассоциированный (сильный) |
| 5 | 25 | Н2О | Ионный ассоциат |
| 0,001 | 25 | С6Н6 | Ассоциированный (слабый) |
Приближенно, для качественных рассуждений можно пользоваться устаревшим делением электролитов на сильные и слабые. Выделение группы электролитов “средней силы” не имеет смысла. Эти электролиты являются ассоциированными. К слабым электролитам обычно относят электролиты, степень диссоцииации которых мала α
Таким образом, к сильным электролитам относятся разбавленные водные растворы почти всех хорошо растворимых в воде солей, многие разбавленные водные растворы минеральных кислот (НСl, HBr, НNО3, НСlO4 и др.), разбавленные водные растворы гидроксидов щелочных металлов. К слабым электролитам принадлежат все органические кислоты в водных растворах, некоторые водные растворы неорганических кислот, например, H2S, HCN, H2CO3, HNO2, HСlO и др. К слабым электролитам относится и вода.
Диссоциация электролитов
Уравнение реакции диссоциации сильного электролита можно представить следующим образом. Между правой и левой частями уравнения реакции диссоциации сильного электролита ставится стрелка или знак равенства:
HCl → H + + Cl —
Допускается также ставить знак обратимости, однако в этом случае указывается направление, в котором смещается равновесие диссоциации, или указывается, что α≈1. Например:
NaOH → Na + + OH —
Диссоциация кислых и основных солей в разбавленных водных растворах протекает следующим образом:
NaHSO3 → Na + + HSO3 —
Анион кислой соли будет диссоциировать в незначительной степени, поскольку является ассоциированным электролитом:
HSO3 — → H + + SO3 2-
Аналогичным образом происходит диссоциация основных солей:
Mg(OH)Cl → MgOH + + Cl —
Катион основной соли подвергается дальнейшей диссоциации как слабый электролит:
MgOH + → Mg 2+ + OH —
Двойные соли в разбавленных водных растворах рассматриваются как неассоциированные электролиты:
Комплексные соединения в разбавленных водных растворах практически полностью диссоциируют на внешнюю и внутреннюю сферы:
В свою очередь, комплексный ион в незначительной степени подвергается дальнейшей диссоциации:
[Fe(CN)6] 3- → Fe 3+ + 6CN —
Константа диссоциации
При растворении слабого электролита К А в растворе установится равновесие:
КА ↔ К + + А —
которое количественно описывается величиной константы равновесия Кд, называемой константой диссоциации :
Kд = [К + ] · [А — ] /[КА] (2)
Константа диссоциации характеризует способность электролита диссоциировать на ионы. Чем больше константа диссоциации, тем больше ионов в растворе слабого электролита. Например, в растворе азотистой кислоты HNO2 ионов Н + больше, чем в растворе синильной кислоты HCN, поскольку К(HNO2) = 4,6·10 — 4 , а К(HCN) = 4,9·10 — 10 .
Для слабых I-I электролитов (HCN, HNO2, CH3COOH) величина константы диссоциации Кд связана со степенью диссоциации α и концентрацией электролита c уравнением Оствальда:
Кд = (α 2· с)/(1-α) (3)
Для практических расчетов при условии, что α
Кд = α 2· с (4)
Поскольку процесс диссоциации слабого электролита обратим, то к нему применим принцип Ле Шателье. В частности, добавление CH3COONa к водному раствору CH3COOH вызовет подавление собственной диссоциации уксусной кислоты и уменьшение концентрации протонов. Таким образом, добавление в раствор ассоциированного электролита веществ, содержащих одноименные ионы, уменьшает его степень диссоциации.
Следует отметить, что константа диссоциации слабого электролита связана с изменением энергии Гиббса в процессе диссоциации этого электролита соотношением:
ΔGT 0 = — RTlnKд (5)
Уравнение (5) используется для расчета констант диссоциации слабых электролитов по термодинамическим данным.
Примеры решения задач
Задача 1. Определите концентрацию ионов калия и фосфат-ионов в 0,025 М растворе K3PO4.
Решение. K3PO4 – сильный электролит и в водном растворе диссоциирует полностью:
Следовательно, концентрации ионов К + и РО4 3- равны соответственно 0,075М и 0,025М.
Задача 2. Определите степень диссоциации αд и концентрацию ионов ОН — (моль/л) в 0,03 М растворе NH3·H2О при 298 К, если при указанной температуре Кд(NH3·H2О) = 1,76× 10 — 5 .
Решение. Уравнение диссоциации электролита:
Концентрации ионов: [NH4 + ] = α С ; [OH — ] = α С , где С – исходная концентрация NH 3 ·H 2 О моль/л. Следовательно:
Kд = αС · αС /(1 — αС)
Кд ≈ α 2 С
Константа диссоциации зависит от температуры и от природы растворителя, но не зависит от концентрации растворов NH 3 ·H 2 О . Закон разбавления Оствальда выражает зависимость α слабого электролита от концентрации.
α = √( Кд / С) = √(1,76× 10 — 5 / 0,03 ) = 0,024 или 2,4 %
[OH — ] = αС, откуда [OH — ] = 2,4·10 — 2 ·0,03 = 7,2·10 -4 моль/л.
Задача 3. Определите константу диссоциации уксусной кислоты, если степень диссоциации CH3CОOH в 0,002 М растворе равна 9,4 %.
Решение. Уравнение диссоциации кислоты:
CH3CОOH → СН3СОО — + Н + .
α = [Н + ] / Сисх(CH3CОOH)
откуда [Н + ] = 9,4·10 — 2 ·0,002 = 1,88·10 -4 М.
Kд = [Н + ] 2 / Сисх(CH3CОOH)
Константу диссоциации можно также найти по формуле: Кд ≈ α 2 С .
Задача 4. Константа диссоциации HNO2 при 298К равна 4,6× 10 — 4 . Найдите концентрацию азотистой кислоты, при которой степень диссоциации HNO2 равна 5 %.
Решение.
Кд = α 2 С , откуда получаем С исх (HNO 2 ) = 4,6·10 — 4 /(5·10 — 2 ) 2 = 0,184 М.
Задача 5. На основе справочных данных рассчитайте константу диссоциации муравьиной кислоты при 298 К.
Решение. Уравнение диссоциации муравьиной кислоты
В “Кратком справочнике физико–химических величин” под редакцией А.А. Равделя и А.М. Пономаревой приведены значения энергий Гиббса образований ионов в растворе, а также гипотетически недиссоциированных молекул. Значения энергий Гиббса для муравьиной кислоты и ионов Н + и СООН — в водном растворе приведены ниже:
| Вещество, ион | НСООН | Н + | СООН — |
| ΔGT 0 , кДж/моль | — 373,0 | 0 | — 351,5 |
Изменение энергии Гиббса процесса диссоциации равно:
ΔGT 0 = — 351,5- (- 373,0) = 21,5 кДж/моль.
Для расчета константы диссоциации используем уравнение (5). Из этого уравнения получаем:
lnKд = — Δ GT 0 /RT= — 21500/(8,31 298) = — 8,68
Откуда находим: Kд = 1,7× 10 — 4 .
Задачи для самостоятельного решения
1. К сильным электролитам в разбавленных водных растворах относятся:
- СН3СOOH
- Na3PO4
- NaCN
- NH3
- C2H5OH
- HNO2
- HNO3
| α = N’/N |
- α=0 — диссоциация отсутствует;
- α=0-3% — слабые электролиты — слабые кислоты (H2SO3, H2S, H2SiO3), слабые основания;
- α=3%-30% — средние электролиты;
- α=30%-100% — сильные электролиты — соли, сильные кислоты (HCl, HBr, HNO3, H2SO4(разб.)), некоторые основания (LiOH, KOH, NaOH);
- α=100% — полная диссоциация.
Степень диссоциации зависит от концентрации раствора.
Константа диссоциации электролита (K) — количественная характеристика диссоциации — отношение произведений концентрации ионов, образованных при диссоциации, к концентрации исходных частиц. Для электролита АВ, который диссоциирует по уравнению АВ↔A — +B + :
| K = ([A — ][B + ]):[AB] |
Константра диссоциации не зависит от концентрации веществ и может колебаться в очень ширком диапазоне — от 10 -16 до 10 15 .
Степень и константа диссоциации связаны между собой соотношением, называемым Законом разведения Оствальда:
| K = ([A — ][B + ]):[AB] = C(α 2 :(1-α)) |
Для слабых электролитов:
| K ≈ α 2 C α ≈ √(K/C) |
Диссоциация воды и её константа диссоциации:
| H2O ↔ H + +OH — K = ([OH — ][H + ]):[H2O] |
Поскольку вода является очень слабым электролитом, то концентрация [H2O] является практически неизменной, поэтому, остаётся постоянной и константа диссоциации воды (ионное произведение воды):
| Kω = [OH — ][H + ] = 10 -14 (при 25°C) |
Для чистой воды:
| [OH — ]=[H + ] = √10 -14 = 10 -7 моль/л |
На практике пользуются водородным показателем pH=-lg[H + ]:
- pH=7 — нейтральная среда;
- pH 7 — щелочная среда.
Диссоциация кислот и оснований
Константа диссоциации одноосновных кислот (Ka-кислотный тип диссоциации; А — -кислотный остаток):
| Kа = ([А — ][H + ]):[HА] |
Многоосновные кислоты диссоциируют в несколько стадий, у каждой из которых своя константа диссоциации.
Константа диссоциации оснований обозначается Kb.
Диссоциация малорастворимых веществ
Константа диссоциации малорастворимых веществ называется произведением растворимости (ПР).
| AgClтв=Ag + +Cl — K = ([Аg + ][Cl — ]):[AgClтв] ПР(AgCl) = [Аg + ][Cl — ] = const |
При наличии в растворе нескольких электролитов они диссоциируют в сторону образования: 1) осадков; 2) газов; 3) слабых электролитов.
Взаимодействие солей с водой с образованием кислой и основной соли называется гидролизом.
Примеры решения задач
Пример 1 . Написать молекулярное уравнение, соответствующее ионному уравнению взаимодействия иона водорода (H + ) с гидроксид-ионом (OH — ).
- ион водорода реагирует с гидроксид-ионом с образованием молекулы воды (реакция нейтрализации):
- ионы водорода образуются при диссоциации сильных кислот (HCl);
- гидроксид-ионы образуются при диссоциации сильных оснований (NaOH);
Пример 2 . Написать молекулярное уравнение, соответствующее ионному уравнению взаимодействия иона водорода с карбонат-ионом.
- карбонат-ионы реагируют с ионами водорода с образованием гидрокарбонат-ионов (реакция протекает при недостатке ионов водорода):
- второй вариант данной реакции — образование неустойчивой угольной кислоты, распадающейся на воду и оксид углерода (протекает при избытке ионов водорода):
- Молекулярные уравнения реакций:
Пример 3 . Написать молекулярное уравнение, соответствующее ионному уравнению взаимодействия иона серебра с гидроксид-ионом.
- ион серебра реагирует с гидроксид-ионом с образованием неустойчивого соединения гидроксида серебра, распадающегося на воду и оксид серебра:
- ионы серебра образуются при диссоциации растворимых солей серебра (AgNO3);
- гидроксид-ионы образуются при диссоциации сильных оснований (NaOH);
Пример 4 . При взаимодействии каких растворов получится карбонат кальция (CaCO3)?
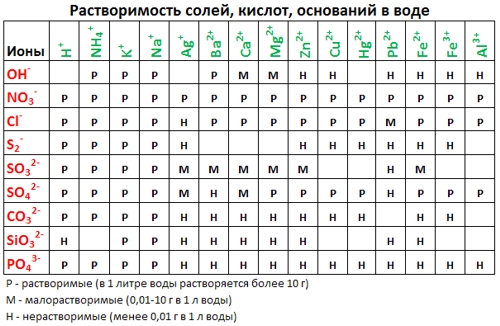
Из таблицы растворимости видно, что карбонат кальция нерастворим в воде.
- Сокращенное ионное уравнение для получения CaCO3 будет иметь следующий вид:
- Для решения задачи подойдет любое растворимое соединение кальция, которое будет диссоциировать с образованием ионов Ca 2+ , например, хлорид или нитрат кальция — CaCl2 или Ca(NO3)2;
- В качестве донора ионов CO3 2- сойдет любой растворимый в воде карбонат, например, Na2CO3 или K2CO3;
- Один из вариантов молекулярного уравнения:
Пример 5 . Растворы каких солей нужны для получения:
Пример 6 . Какие вещества образуются при взаимодействии растворов сульфата натрия (Na2SO4) и хлорида бария (BaCl2)?
- Из таблицы растворимости видно, что обе соли растворимы в воде:
- При слиянии растворов образуются катионы натрия и бария и анионы хлора и оксида серы. Из таблицы растворимости видно, что нерастворимую в воде соль даст сочетание Ba 2+ и SO4 2- :
- Уравнение реакции будет иметь вид:
Пример 7 . Какая соль выпадет в осадок при взаимодействии нитрата серебра (AgNO3) и хлорида кальция (CaCl2)? Написать уравнение реакции.
Пример 8 . Каким образом можно очистить поваренную соль (NaCl) от сульфата натрия (Na2SO4)?
Идея решения задачи заключается в добавлении в раствор поваренной соли и сульфата натрия вещества, способного распадаться на ионы, которые свяжут ионы оксида серы в нерастворимую соль, высвободив тем самым ионы натрия.
Роль связывающего вещества выполнит хлорид кальция CaCl2.
После того, как CaSO4↓ выпадет в осадок, полученный раствор необходимо будет отфильтровать, после чего в фильтрате будет присутствовать чистая поваренная соль.
Пример 9 . Написать молекулярное и ионное уравнение реакции хлорида алюминия с нитратом серебра.
- Молекулярное уравнение:
- Полное ионное уравнение:
- Сокращенное ионное уравнение:
Пример 10 . Рассчитать концентрацию ионов, образующихся при смешении 1 литра 0,25М раствора BaCl2 и 1 литра 0,5М раствора Na2SO4, после выпадения BaSO4 в осадок.
- Молекулярное уравнение реакции:
- Сокращенное ионное уравнение:
- Рассчитаем исходные кол-ва ионов:
- (Ba 2+ ) в обменной реакции присутствует в недостатке, поэтому, в реакцию вступает не 0,5, а только 0,25 SO4 2- ;
- Объем полученного раствора 1+1=2 литра;
- Рассчитаем молярные концентрации ионов:
Пример 11 . Рассчитать pH водного раствора 0,1М HCl; 0,1M NaOH.
- HCl — сильная кислота, диссоциирует полностью, уравнение диссоциации:
- NaOH — сильное основание, диссоциирует полностью, уравнение диссоциации:
Пример 12 . Рассчитать концентрацию ионов водорода в растворе аммиака с концентрацией 1,5 моль/л (K=1,7·10 -5 ).
- Формула равновесия, установленного в водном растворе аммиака:
- Обозначим через x равновесную концентрацию [OH — ]; тогда [NH4 + ]=x; [NH3]=1,5-x:
Пример 13 . Какое кол-во осадка образуется при смешении 250 мл растворов нитрита лития (концентрация 0,3 моль/л) и фторида натрия (0,2 моль/л), если произведение растворимости фторида лития ПР(LiF)=1,5·10 -3 .
- Уравнение реакции:
- Рассчитаем исходные кол-ва ионов:
- Объем раствора равен 0,25+0,25=0,5 л
- Если обозначить через x моль кол-во выпавшего осадка LiF, тогда произведение концентрации ионов в растворе будет равно:
- Масса выпавшего осадка:
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе