Большинство органических соединений имеют молекулярное строение. Атомы в веществах с молекулярным типом строения всегда образуют только ковалентные связи друг с другом, что наблюдается и в случае органических соединений. Напомним, что ковалентным называется такой вид связи между атомами, который реализуется за счет того, что атомы обобществляют часть своих внешних электронов с целью приобретения электронной конфигурации благородного газа.
По количеству обобществлённых электронных пар ковалентные связи в органических веществах можно разделить на одинарные, двойные и тройные. Обозначаются данные типы связей в графической формуле соответственно одной, двумя или тремя чертами:
Кратность связи приводит к уменьшении ее длины, так одинарная С-С связь имеет длину 0,154 нм, двойная С=С связь – 0,134 нм, тройная С≡С связь – 0,120 нм.
- Типы связей по способу перекрывания орбиталей
- Как узнать, когда в молекуле есть π- и ϭ-связи?
- Гибридизация орбиталей атома углерода
- Как определить тип гибридизации атома углерода в органической молекуле?
- Радикал. Функциональная группа
- Химия, Биология, подготовка к ГИА и ЕГЭ
- Одинарная, двойная и тройная связи, а- и я-связь
Типы связей по способу перекрывания орбиталей
Как известно, орбитали могут иметь различную форму, так, например, s-орбитали имеют сферическую, а p-гантелеобразную форму. По этой причине связи также могут отличаться по способу перекрывания электронных орбиталей:
• ϭ-связи – образуются при перекрывании орбиталей таким образом, что область их перекрывания пересекается линией, соединяющей ядра. Примеры ϭ-связей:
• π-связи – образуются при перекрывании орбиталей, в двух областях – над и под линией соединяющей ядра атомов. Примеры π-связей:
Как узнать, когда в молекуле есть π- и ϭ-связи?
При ковалентном типе связи ϭ-связь между любыми двумя атомами есть всегда, а π-связь имеет только в случае кратных (двойных, тройных) связей. При этом:
- Одинарная связь – всегда является ϭ-связью
- Двойная связь всегда состоит из одной ϭ- и одной π-связи
- Тройная связь всегда образована одной ϭ- и двумя π-связями.
Укажем данные типы связей в молекуле бутин-3-овой кислоты:
Гибридизация орбиталей атома углерода
Гибридизацией орбиталей называют процесс, при котором орбитали, изначально имеющие разные формы и энергии смешиваются, образуя взамен такое же количество гибридных орбиталей, равных по форме и энергии.
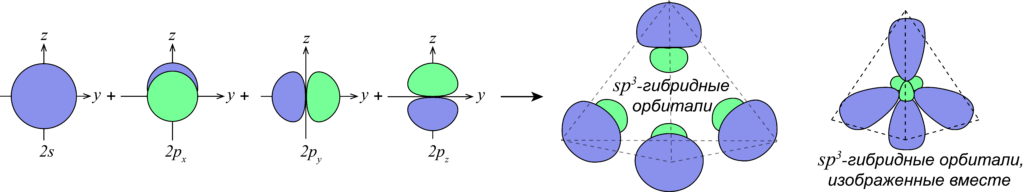
Так, например, при смешении одной s- и трех p-орбиталей образуются четыре sp 3 -гибридных орбитали:
В случае атомов углерода в гибридизации всегда принимает участие s-орбиталь, а количество p-орбиталей, которые могут принимать участие в гибридизации варьируется от одной до трех p-орбиталей.
Как определить тип гибридизации атома углерода в органической молекуле?
В зависимости от того, со скольким числом других атомов связан какой-либо атом углерода, он находится либо в состоянии sp 3 , либо в состоянии sp 2 , либо в состоянии sp-гибридизации:
| Количество атомов, с которыми связан атом углерода | Тип гибридизации атома углерода | Примеры веществ |
| 4 атома | sp 3 | CH4 – метан |
| 3 атома | sp 2 | H2C=CH2 – этилен |
| 2 атома | sp | HC≡CH — ацетилен |
Потренируемся определять тип гибридизации атомов углерода на примере следующей органической молекулы:
- Первый атом углерода связан с двумя другими атомами (1H и 1C), значит он находится в состоянии sp-гибридизации.
- Второй атом углерода связан с двумя атомами – sp-гибридизация
- Третий атом углерода связан с четырьмя другими атомами (два С и два Н) – sp 3 -гибридизация
- Четвертый атом углерода связан с тремя другими атомами (2О и 1С) – sp 2 -гибридизация.
Радикал. Функциональная группа
Под термином радикал, чаще всего подразумевают углеводородный радикал, являющийся остатком молекулы какого-либо углеводорода без одного атома водорода.
Название углеводородного радикала формируется, исходя из названия соответствующего ему углеводорода заменой суффикса –ан на суффикс –ил.
| Формула углеводорода | Название углеводорода | Формула радикала | Название радикала |
| CH4 | метан | -CH3 | метил |
| C2H6 | этан | -С2Н5 | этил |
| C3H8 | пропан | -С3Н7 | пропил |
| СnН2n+2 | …ан | -СnН2n+1 | … ил |
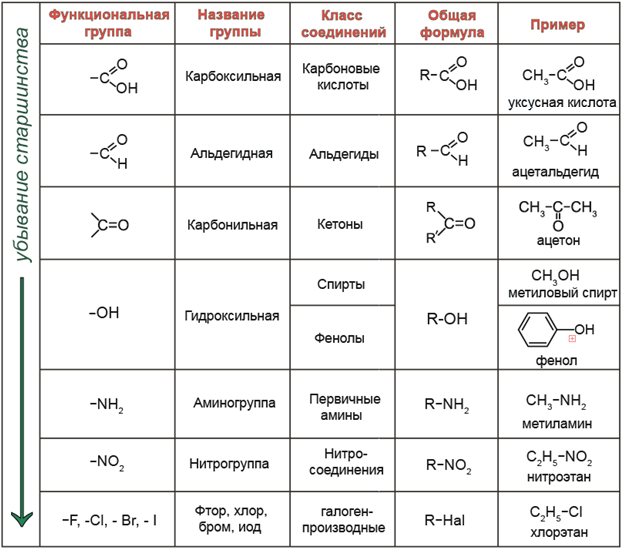
Функциональная группа — структурный фрагмент органической молекулы (некоторая группа атомов), который отвечает за её конкретные химические свойства.
В зависимости того, какая из функциональных групп в молекуле вещества является старшей, соединение относят к тому или иному классу.
R – обозначение углеводородного заместителя (радикала).
Радикалы могут содержать кратные связи, которые тоже можно рассматривать как функциональные группы, поскольку кратные связи вносят вклад в химические свойства вещества.
Если в молекуле органического вещества содержится две или более функциональных группы, такие соединения называют полифункциональными.
Химия, Биология, подготовка к ГИА и ЕГЭ
Задание А3 ГИА (ОГЭ) по химии —
ковалентная полярная и ковалентная неполярная, ионная, металлическая
1. Одинарная, двойная и тройная
Как известно, химическая связь это образование общей электронной пары между атомами (один от одного атома, другой от другого).
Если электронов несколько, то и связей больше, чем одна.
Валентность элементов главных подгрупп Периодической системы зависит от числа электронов, находящихся на внешнем электронном слое. Поэтому эти внешние электроны принято называть валентными. Для элементов побочных подгрупп в качестве валентных электронов могут выступать как электроны внешнего слоя, так и электроны внутренних подуровней.
- атомы одновалентных элементов образуют одинарную связь:
- двухвалентные — двойную: O2: O=O
- если валентность = 3, то тройную: N2: N≡N
И это применимо не только к простым веществам.
- если у атома валентность = 1, то он будет проявлять ее и в сложных веществах — образовывать три связи:
- у S, как и у О валентность равна двум: H2O: это могут быть две одинарнеы связи: H-O-H или двойные: CO: C=O
- N, P, B и т.д. — 3: NH3 — три одинарные связи, HCN: H-C≡N — тройная связь
Ответ: 3) NH3 — три одинарные свзи
Ответ: 3) O2 — двойная связь
2. Ковалентная, ионная и т.д. …
- ковалентную связь образуют: неметаллы, неметаллы и водород;
- ионную — металлы и неметаллы, катионы ( в том числе и NH4+) и кислотные остатки;
- металлическую — металлы
1) PCl5 — два разных неметалла, значит, связь полярная ковалентная
2) CaCl2 — металл и неметалл, следовательно, ионная
3) Cl2 — два одинаковых неметалла — неполярная ковалентная
4) KCl — металл и неметалл, следовательно, ионная
Ответ: 1) PCl5
1) оксид серы — два неметалла, значит, будет ковалентная связь;
2) оксид бария — металл и неметалл — ионная
3) сероводород — неметалл и водород — ковалентная
4) аммиак — аналогично
Ответ: 2) BaO
1) все вещества образованы разными неметаллами и водородом — ковалентная поярная;
2) все вещества простые — значит, связь неполярная ковалентная
3) все вещества ионные
4) хлороводород и фосфин — ковалентная связь, соль — ионная
Ответ: 1)
Здесь важна последовательность — чтобы первое вещество было с ковалентной. а второй — с ионной, не наоборот. Такие каверзы редко, но встречаются в заданиях ГИА (ОГЭ).
1) Оксид фосфора — полярная ковалентная, оксид натрия — ионная;
2) хлорид натрия — ионная, хлор — ковалентная;
3) азот — ковалентная, неполярная, сульфид натрия — ионная;
4) хлорид кальция — ионная, хлороводород — ковалентная полярная
Одинарная, двойная и тройная связи, а- и я-связь
В рассмотренных примерах образования химической связи принимала участие электронная пара. Такая связь называется одинарной. Иногда ее называют ординарной, т.е. обычной. Этот тип связи принято обозначать одной черточкой, соединяющей символы взаимодействующих атомов.
Перекрывание электронных облаков по прямой линии, соединяющей два ядра, приводит к сигма-связи (о-связь). Одинарная связь в большинстве случаев является а-связью.
Связь, образованная перекрыванием боковых областей р-элект- ронных облаков, называется пи-связыо (я-связь). Двойная и тройная связи образуются при участии соответственно двух и трех электронных пар. Двойная связь представляет собой одну а-связь и одну я-связь, тройная связь — одну a-связь и две я-связи.
Обсудим образование связей в молекулах этана С2Н6, этилена С2Н4, ацетилена С2Н2 и бензола С6Нб.
Углы между связями в молекуле этана С.;Н(. почти точно равны между собой (рис. 1.18, а) и не отличаются от углов между связями С—Н в молекуле метана. Поэтому можно предположить, что наружные электронные оболочки атомов углерода находятся в состоянии $р 3 -гибридизации. Молекула С2Н6 диамагнитна и не имеет электрического момента диполя. Энергия связи С—С равна -335 кДж/моль. Все связи в молекуле С9Н6 — а-связи.
В молекуле этилена С2Н4 углы между связями равны примерно по 120°. Из этого можно сделать вывод о $р 2 -гибридизации наружных электронных орбиталей атома углерода (рис. 1.18, б). Связи С—Н лежат в одной плоскости под углами около 120°. У каждого атома углерода имеется по одной негибридной р-орбитали, содер-
Рис. 1.18. Модели молекул этана (а), этилена (б) и ацетилена (в)
жащей по одному электрону. Эти орбитали расположены перпендикулярно плоскости рисунка.
Энергия связи между атомами углерода в молекуле этилена С2Н4 равна -592 кДж/моль. Если бы атомы углерода были связаны такой же связью, как в молекуле этана, то энергии связи в этих молекулах были бы близки.
Однако энергия связи между атомами углерода в этане составляет 335 кДж/моль, что почти в два раза меньше, чем в этилене. Столь существенная разница в энергиях связи между атомами углерода в молекулах этилена и этана объясняется возможным взаимодействием негибридных р-орбиталей, что на рис. 1.18, б изображено волнистыми линиями. Связь, образованная таким способом, и называется я-связью.
В молекуле этилена С2Н4 четыре связи С—Н, как и в молекуле метана СН4, являются a-связями, а связь между атомами углерода представляет собой a-связь и л-связь, т.е. двойную связь, и формула этилена записывается как Н2С=СН2.
Молекула ацетилена С2Н2 линейная (рис. 1.18, в), что говорит в пользу sp-гибридизации. Энергия связи между атомами углерода равна -811 кДж/моль, что позволяет предположить существование одной a-связи и двух л-связей, т.е. это тройная связь. Формула ацетилена записывается как НС=СН.
Один из сложных вопросов химии состоит в установлении природы связей между атомами углерода в так называемых ароматических соединениях, в частности в молекуле бензола С6Н(.. Молекула бензола плоская, углы между связями атомов углерода равны по
Рис. 1.19. Модели молекулы бензола:
а — формульная модель: 6 — ^-орбитали атомов углерода и a-связи между атомами углерода и атомами углерода и водорода; в — p-обитали и л-связи между
120°, что позволяет предположить .^-гибридизацию внешних орбиталей атомов углерода. Обычно молекулу бензола изображают, как это показано на рис. 1.19, а.
Казалось бы, в бензоле связь между атомами углерода должна быть длиннее двойной связи С=С как более прочной. Однако изучение структуры молекулы бензола показывает, что все расстояния между атомами углерода в бензольном кольце одинаковы.
Эта особенность молекулы лучше всего объясняется тем, что негибридные р-орбитали всех атомов углерода перекрываются «боковыми» частями (рис. 1.19, б), поэтому все межъядерные расстояния между атомами углерода равны. На рис. 1.19, в показаны а-связи между атомами углерода, образованные перекрыванием sp 2 —гибридных орбиталей.
Энергия связи между атомами углерода в молекуле бензола С6Н6 равна -505 кДж/моль, и это позволяет предположить, что эти связи являются промежуточными между одинарной и двойной связями. Заметим, что электроны р-орбиталей в молекуле бензола двигаются по замкнутому шестиугольнику, и они делокализованы (не относятся к некоторому определенному месту).