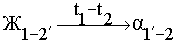Научиться анализировать фазовые превращения при охлаждении сплавов двойных систем: твердых растворов, эвтектического типа; изображать схемы микроструктур сплавов.
Микроструктура сплава формируется в процессах кристаллизации расплава, фазовых превращений и структурных изменений в твердом состоянии, происходящих при литье, обработке давлением и термической обработке.
Несмотря на многообразие факторов, влияющих на формирование микроструктуры сплава, важнейшие ее особенности можно предсказать, используя диаграмму состояния, так как именно диаграмма состояния дает сведения о характере фазовых превращений и их последовательности при нагревании и охлаждении сплава. Вместе с тем следует помнить, что диаграмма состояния описывает фазовое состояние в равновесных условиях, а реальная структура сплава складывается во времени и в неравновесных условиях (при ускоренном охлаждении, при больших степенях пластической деформации и т.д.).
Далее приведены сведения о типичных структурах, которые необходимо знать, прежде чем приступить к изучению микростроения промышленных сплавов.
СИСТЕМА С НЕОГРАНИЧЕННОЙ РАСТВОРИМОСТЬЮ
КОМПОНЕНТОВ В ЖИДКОМ И ТВЕРДОМ СОСТОЯНИЯХ
Диаграмма состояния двойной системы с неограниченной растворимостью компонентов в жидком и твердом состояниях представлена на рис. 1.
Рис. 1. Диаграмма состояния сплавов, компоненты которых полностью растворимы
в жидком и твердом состоянии и кривая охлаждения сплава Х.
Верхнюю кривую на диаграмме называют линией ликвидуса. Выше этой линии все сплавы системы А-В однофазны и находятся в жидком состоянии (Ж). Нижнюю кривую диаграммы называют линией солидуса. При температурах ниже этой линии все сплавы однофазны и состоят из кристаллов a-раствора. В интервале температур между кривыми ликвидуса и солидуса, называемом интервалом кристаллизации, или интервалом плавления, все сплавы состоят из двух фаз: жидкости и кристаллов a-раствора.
Кривые ликвидуса и солидуса – это геометрическое место точек, отвечающих температурам начала и конца кристаллизации различных сплавов системы А-В. Кроме того, эти кривые отображают составы равновесных фаз (Ж и a) в различных сплавах и интервале их кристализации, т.е. изображают составы насыщенных один относительно другого жидких и твердых растворов.
Рассмотрим процесс кристаллизации сплава Х. При температуре выше t1 (температура начала кристаллизации) этот сплав представляет собой ненасыщенный жидкий раствор. Как только температура сплава понизится с температуры t1, жидкий раствор станет насыщенным относительно a-кристаллов и понижение температуры ниже t1 приведет к выделению из жидкости состава точки 1 первичных кристаллов a-раствора состава точки 1’, расположенной на кривой солидуса. Составы жидкости и выпавших из нее a-кристаллов изменяются при понижении температуры от t1 до t2 в соответствии с кривыми ликвидуса и солидуса: жидкость – от точки 1 до точки 2’, a-кристалл – от точки 1’ до 2. Следовательно, в интервале кристаллизации в объемах сосуществующих фаз должна протекать выравнивающая диффузия. Рассмотренный процесс первичной кристаллизации сплава Х можно записать как:
При температуре конца кристаллизации (t2) последние следы жидкой фазы (состава точки 2’) исчезнут и сплав будет состоять из a-кристаллов (состава точки 2). При охлаждении от температуры t2до комнатной в сплаве не происходит фазовых превращений. После равновесной кристаллизации структура сплава Х будет состоять из кристаллов твердого раствора a, состав которых соответствует составу сплава (рис. 2). Зерна под микроскопом могут иметь неодинаковый цвет (более темный или более светлый), т.к. в сечении шлифа попадают различные кристаллографические плоскости по-разному ориентированные в пространстве кристаллов. Аналогичную структуру будут иметь все однофазные сплавы, а также чистые компоненты. Поэтому по структуре однофазного материала после равновесной кристаллизации нельзя определить что это: сплав, раствор или чистый металл. Форма и размеры зерен не являются специфическими для того или иного сплава, а зависят от условий кристаллизации.
Рис. 2. Схема структуры однофазного сплава Х.
При температуре tе в системе А-В (рис. 3, 4) протекает эвтектическое превращение
Это превращение происходит во всех сплавах, расположенных по составу между точками а и b. Горизонталь аb и точку е на этой горизонтали называют эвтектическими, а смесь кристаллов (aа + bb), которые выделяется из жидкости при эвтектической кристаллизации, – эвтектикой.
Кривые аа1 и bb1, показывающие как изменяется растворимость одного компонента в другом в твердом состоянии при понижении температур от эвтектической до комнатной, называют сольвусами a и b – твердых растворов.
Сплавы, расположенные левее точки е, называют доэвтектическими. Сплавы, расположенные правее точки е – заэвтектическими. Сплав, состава точки е, называют эвтектическим, или просто эвтектикой.
Рис. 3. Фазовая диаграмма состояния сплавов, компоненты которых ограничено
растворимы в твердом состоянии и образуют эвтектику.
Рис. 4. Структурная диаграмма состояния сплавов, компоненты которых ограничено
растворимы в твердом состоянии и образуют эвтектику.
Кристаллизация граничных a и b – растворов в сплавах, состав которых находится в интервале А-а1 и В-b1, протекает также, как сплав системы с неограниченной растворимостью компонентов в жидком и твердом состояниях. Эти сплавы однофазны, поэтому их структура аналогична структуре, представленной на рис. 2.
Сплавы, состав которых находится в интервалах а1с и db1, не претерпевают эвтектического превращения. Рассмотрим процессы фазовых превращений на примере сплава Х1. В интервале температур t1 – t2 сплав Х1 кристаллизуется как граничный a – твердый раствор, идет первичная кристаллизация.
При охлаждении от температуры t2до температуры t3 в нем не протекают никакие фазовые превращения. Как только фигуративная точка сплава окажется на кривой сольвуса аа1, граничный a – раствор состава точки 3 станет насыщенным относительно граничного твердого раствора b состава точки 3’. Поэтому при дальнейшем понижении температуры от t3 до комнатной из a – кристаллов, изменяющих свой состав по кривой 3а1, выделяются вторичные кристаллы b – фазы, состав которых будет изменяться по кривой 3’ b1. Этот процесс можно записать так:
При комнатной температуре кристаллы a-фазы состава а1 окажутся в равновесии с кристаллами b состава b1. Доля обеих фаз по правилу рычага измеряется отношением отрезков.
Под микроскопом в структуре сплава Х1 можно увидеть кристаллы двух видов: первичные кристаллы a – раствора (основа сплава) и вторичные b –кристаллы. Вторичные выделения образуются по границам и внутри зерен исходной фазы a. Вторичные выделения обычно имеют пластинчатую или иглообразную форму, иногда они имеют вид тонких прослоек или компактных частиц, располагающихся по границам первичных зерен (рис. 5).
В сплаве Х1имеются две структурные составляющие первичные кристаллы a – фазы и вторичные кристаллы b. Под структурными составляющими в сплавах понимают такие самостоятельные элементы их микроструктуры, которые при рассмотрении под микроскопом имеют свое характерное однородное строение. Для сплава Х1 понятие “структурная составляющая” и “фаза” совпадают, поскольку каждая из его структурных составляющих – это одновременно a или b – фаза.
Рис. 5. Схемы структуры сплава Х1 с вторичными выделениями пластинчатой формы
(а), в виде тонких прослоек (б) или компактных частиц (в)
Более сложную структуру имеют до – и заэвтектические сплавы, в которых помимо первичных a – или b – кристаллов, выделяется эвтектика 
В заэвтектическом сплаве Х2 процесс первичной кристаллизации пройдет по схеме:

Из оставшейся жидкости Же выделяется эвтектика – смесь кристаллов (aа+bb), т. е. 
По окончании кристаллизации сплав Х2 состоит из первичных кристаллов bb, эвтектики (aа+bb). Так как при эвтектической температуре сплав Х2 состоит из кристаллов предельно насыщенных aа— и bb-растворов, а с понижением температуры взаимная растворимость компонентов в твердом состоянии уменьшается, то при охлаждении до комнатной температуры их b –кристаллов (первичных и эвтектических) будут выделяться вторичные a –кристаллы, а из эвтектических a –кристаллов – соответственно вторичные b –кристаллы.
Возможные варианты микроструктуры сплава Х2 показаны на рис. 6.
Рис. 6. Схемы структур заэвтектического сплава Х2 с эвтектикой и первичными
кристаллами в форме многогранников (а) и дендритов (б).
Первичные b – кристаллы могут иметь четкую огранку (рис. 6а) или дендритную форму (рис. 6б). Вокруг первичных b – кристаллов видна вторая структурная составляющая – эвтектика (a + b), имеющая пластинчатое или другое строение. Внутри первичных кристаллов b в небольшом количестве находится третья структурная составляющая – вторичные a –кристаллы. Выделения вторичных кристаллов в эвтектике незаметны, так как сама эвтектика достаточно дисперсная смесь двух видов кристаллов. Структура других заэвтектических сплавов аналогична разобранной. Различие состоит лишь в соотношении объемов в структурных составляющих.
1. Название работы.
3. Изображение диаграмм состояния двойных систем с нанесением ординат заданных сплавов.
4. Кривые охлаждения этих сплавов.
5. Схемы микроструктур сплавов.
КОНТРОЛЬНЫЕ ВОПРОСЫ ДЛЯ САМОПРОВЕРКИ
1. Опишите процесс первичной кристаллизации в сплавах – твердых растворах.
2. Какова микроструктура однофазного сплава после равновесной кристаллизации?
3. Как определить долю эвтектики и первичных кристаллов по диаграмме состояния?
4. Что такое эвтектика? Какое строение она имеет?
5. Какие структурные составляющие имеют до и заэвтектические сплавы?
6. Какова возможная форма выделений вторичных кристаллов?
ИЗУЧЕНИЕ ДИАГРАММЫ СОСТОЯНИЯ
ЖЕЛЕЗОУГЛЕРОДИСТЫХ СПЛАВОВ
Изучить диаграмму состояния железоуглеродистых сплавов. Разобраться с превращениями, происходящими в железоуглеродистых сплавах при медленном охлаждении и нагреве.
Диаграмма состояния системы Fe – Fe3C.
Фотографии микроструктур железоуглеродистых сплавов.
Диаграмма железоуглеродистых сплавов может быть представлена в двух вариантах: метастабильном, отражающем превращения в системе “железо-карбид железа”, и стабильном, отражающем превращения в системе “железо-графит”. Наибольшее практическое значение имеет диаграмма состояния “железо-карбид железа”, т.к. для большинства технических сплавов превращения реализуются по этой диаграмме.
Карбид железа (Fe3C) называют цементитом, поэтому метастабильную диаграмму железоуглеродистых сплавов называют диаграммой состояния “железо-цементит” (Fe-Fe3C).
Компоненты и фазы в железоуглеродистых сплавах
Основными компонентами железоуглеродистых сплавов являются железо и углерод, которые относятся к полиморфным элементам. В железоуглеродистых сплавах эти элементы взаимодействуют, образуя различные фазы. Под фазой в общем смысле понимается однородная часть системы, имеющая одинаковый химический состав, физические свойства и отделенная от других частей системы поверхностью раздела. Взаимодействие железа и углерода состоит в том, что углерод может растворяться как в жидком (расплавленном) железе, так и в различных его модификациях в твердом состоянии. Помимо этого он может образовывать с железом химическое соединение. Таким образом в железоуглеродистых сплавах могут образовываться следующие фазы: жидкий раствор, аустенит, феррит, цементит.
Аустенит (обозначают A или g) – твердый раствор внедрения углерода в Feg. Имеет ГЦК – решетку, растворяет углерода до 2,14 %, немагнитен, твердость (HB 160-200).
Феррит (обозначают Ф или a) – твердый раствор внедрения углерода в Fea. Имеет ОЦК – решетку, растворяет углерода до 0,02 % (727 °C), при 20 °C менее 0,006 %, ферромагнитен до температуры 769 °C, твердость (HB 80-100).
Цементит (Ц) – химическое соединение железа с углеродом (Fe3C). Содержит 6,67 % C. При нормальных условиях цементит тверд (HB 800) и хрупок. Слабо ферромагнитен до 210 °C.
Превращения в железоуглеродистых сплавах
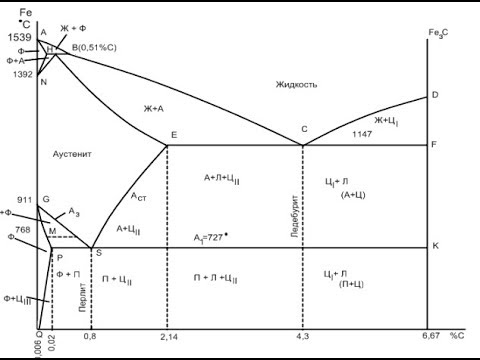
Диаграмма состояния Fe-Fe3C (рис. 1) показывает фазовый состав и превращения в сплавах с концентрацией от чистого железа до цементита.
Превращения в железоуглеродистых сплавах происходит как при кристаллизации (затвердевании) жидкой фазы (Ж), так и в твердом состоянии.
Рис. 1. Диаграмма состояния Fe – Fe3C (в упрощенном виде).
Первичная кристаллизация идет в интервале температур, ограни-ченных линиями ликвидус (ACD) и солидус (AECF).
Вторичная кристаллизация происходит за счет превращения железа одной аллотропической модификации в другую и за счет изменения растворимости углерода в аустените и феррите, которая уменьшается с понижением температуры. Избыток углерода выделяется из твердых растворов в виде цементита. В сплавах системы Fe-Fe3C происходят следующие изотермические превращения:
Эвтектическое превращение на линии ECF (1147 °C)
Эвтектоидное превращение на линии PSK (727 °C)
Эвтектическая смесь аустенита и цементита называется ледебуритом(Л), а эвтектоидная смесь феррита и цементита – перлитом(П). Ледебурит содержит 4,3 % углерода. При охлаждении ледебурита ниже линий PSK входящий в него аустенит превращается в перлит и при нормальной температуре ледебурит представляет собой смесь перлита и цементита и называется ледебуритом превращенным (Л пр). Цементит в этой структурной составляющей образует сплошную матрицу, в которой размещены колонии перлита. Такое строение ледебурита объясняет его большую твердость (HB 700) и хрупкость.
Перлит содержит 0,8 % углерода. В зависимости от формы частичек цементит бывает пластинчатый и зернистый. Является прочной структурной составляющей с твердостью (HB210).
Линии диаграммы состояния Fе – Fе3C
Линии диаграммы представляют собой совокупность критических точек сплавов с различным составом, характеризующих превращения в этих сплавах при соответствующих температурах.
Рассмотрим значение линий диаграммы при медленном охлаждении.
ACD – линия ликвидус. Выше этой линии все сплавы находятся в жидком состоянии.
AECF – линия солидус. Ниже этой линии все сплавы находятся в твердом состоянии.
АС – из жидкого раствора выпадают кристаллы аустенита.
CD – линия выделения первичного цементита.
AE – заканчивается кристаллизация аустенита.
ECF – линия эвтектического превращения.
GS – определяет температуру начала выделения феррита из аустенита (910-727 °C).
GP – определяет температуру окончания выделения феррита из аустенита.
PSK – линия эвтектоидного превращения.
ES – линия выделения вторичного цементита.
PQ – линия выделения третичного цементита.
Области диаграммы состояния Fe – Fe3C
Линии диаграммы: делят все поле диаграммы на области равновесного существования фаз. Каждой области диаграммы соответствует определенное структурное состояние, сформированное в результате происходящих в сплавах превращений.
I – Жидкий раствор (Ж).
II –Жидкий раствор (Ж) и кристаллы аустенита (А).
III – Жидкий раствор (Ж) и кристаллы цементита первичного (ЦI).
IV – Кристаллы аустенита (А).
V – Кристаллы аустенита (А) и феррита (Ф).
VI – Кристаллы феррита (Ф).
VII – Кристаллы аустенита (А) и цементита вторичного (ЦII).
VIII – Кристаллы феррита (Ф) и цементита третичного (ЦIII).
IX – Кристаллы феррита (Ф) и перлита (П).
X – Кристаллы перлита (П) и цементита вторичного (ЦII).
XI – Кристаллы аустенита (А), ледебурита (Л) и цементита вторичного (ЦII).
XII – Кристаллы перлита (П), цементита вторичного (ЦII) и ледебурита превращенного (Л пр).
XIII –Кристаллы ледебурита и цементита первичного (ЦI).
XIV – Кристаллы цементита первичного (ЦI) перлита (П) и ледебурита превращенного (Л пр).
1. Название работы.
2. Цель работы.
3. Диаграмма состояния Fe – Fe3C с обозначением фаз и структурных состовляющих по всем областям диаграммы.
4. Характеристика линий и структурных составляющих железоуглеродистых сплавов.
5. Подробное описание изменений структуры при медленном охлаждении контрольного сплава. (Фрагмент диаграммы с контрольным сплавом).
Рис. 2. Фрагмент диаграммы состояния Fe – Fe3C с нанесенной ординатой
состава сплава, содержащего 1,3 % C.
6. Схема микроструктуры контрольного сплава при нормальной температуре.
7. Выводы.
КОНТРОЛЬНЫЕ ВОПРОСЫ ДЛЯ САМОПРОВЕРКИ
1. Что такое фаза?
2. Что такое аустенит?
3. Что такое феррит?
4. Что такое цементит?
5. Какими линиями диаграммы ограничивается температурный интервал первичной кристаллизации?
6. В чем состоит сущность эвтектического превращения?
7. В чем состоит сущность эвтектоидного превращения?
8. Что такое ледебурит?
9. Что такое перлит?
10. На какой линии происходят эвтектические превращения?
11. На какой линии происходят эвтектоидные превращения?
12. Линия выделения первичного цементита?
13. Линия выделения вторичного цементита?
14. Линия выделения третичного цементита?
15. Назовите фазы железоуглеродистых сплавов.
16. Максимальное растворение углерода в Fea?
17. Максимальное растворение углерода в Feg?
18. Содержание углерода в цементите?
19. При какой температуре происходит эвтектическое превращение?
20. При какой температуре происходит эвтектоидное превращение?
Видео:Лекция «Диаграмма состояния двухкомпонентных сплавов»Скачать

Диаграмма состояния сплавов, компоненты которых образуют смеси
Приведем построение такой диаграммы на примере системы «свинец – сурьма» («Рb – Sb»). Кривые охлаждения компонентов и сплавов представлены на рис. 3.4.
Рис. 3.4. Кривые охлаждения сплавов системы «Pb – Sb«
Критические точки для чистых металлов и сплавов приведены в табл. 3.1.
Критические точки сплавов системы «Pb – Sb»
Химический состав, % масс.
Температура кристаллизации, °С (критические точки)
На основании анализа кривых охлаждения (см. рис. 3.4 и табл. 3.1) построим диаграмму состояния «Pb – Sb».
На оси абсцисс отмечают точки, соответствующие составам исследованных сплавов, и указывают температуры начала и конца кристаллизации этих сплавов. Соединив температуры начала кристаллизации сплавов с температурами кристаллизации чистых компонентов, получим линию, которая называется ликвидус – линия АСВ диаграммы (рис. 3.5, а). Выше нее все сплавы находятся в жидком состоянии.
Рис. 3.5. Диаграмма состояния «Pb – Sb»:
а – фазовая; б – структурная
Соединив точки окончания кристаллизации сплавов, получим линию солидус – линия DCE диаграммы, ниже которой все сплавы находятся в твердом состоянии. Линию солидус не следует проводить до осей ординат, так как всегда существует некоторая весьма малая взаимная растворимость компонентов системы (области, ограниченные пунктирными линиями), которой обычно пренебрегают.
На фазовой диаграмме системы «свинец – сурьма» указаны только фазы – их три в данной системе. Это жидкая фаза и две твердых – свинец и сурьма.
Фазовые диаграммы не дают представления о структуре сплавов, а следовательно, не позволяют судить об их свойствах. Более полную информацию о сплавах дают структурные диаграммы состояния (рис. 3.5, б). Для построения такой диаграммы необходимо рассмотреть превращения, которые происходят в чистых металлах (компонентах) и в характерных сплавах данной системы. Это прежде всего сплав, химический состав которого 87% Рb и 13% Sb (I), а также сплавы с меньшим (II) и большим (III) содержанием сурьмы.
Чистые металлы – свинец и сурьма кристаллизуются при постоянной температуре (горизонтальные участки (1–1′) на кривых охлаждения (см. рис 3.4)). Как указывалось выше, это соответствует правилу фаз. Действительно, число компонентов (К) равно единице (чистый металл), количество фаз (Ф) при кристаллизации две – жидкая и твердая, а число степеней свободы (С) равно нулю (С = К – Ф+1 = 1 – 2 + 1 = 0). Это означает, что кристаллизация должна проходить при постоянной температуре.
Кристаллизация всех сплавов, кроме одного (87% РЬ, 13% Sb), протекает в интервале температур. Особое положение занимает сплав I (87% РЬ, 13% Sb), который, так же как чистые металлы, кристаллизуется при постоянной температуре.
Рассмотрим кристаллизацию этого сплава. Участок 0–1 кривой охлаждения сплава (см. рис. 3.4, г) соответствует охлаждению жидкости (К = 2, Ф = 1 – одна фаза – жидкость, т.е. С = 1, поэтому возможно изменение температуры при сохранении фазового состава). При температуре 246 °С (линия DBE диаграммы, (рис. 3.5, б)) происходит кристаллизация жидкости при постоянной температуре (участок 1–1′ на кривой охлаждения), т.е. С = 0. При К = 2 такое возможно только в том случае, если Ф = 3, тогда С = 2- 3+ 1 = = 0. Это означает, что при кристаллизации сплава одновременно существуют три фазы (жидкость, свинец и сурьма), т.е. из жидкости одновременно выделяются оба компонента, образуя смесь.
Такой наиболее легкоплавкий сплав системы и называется эвтектическим, а структура, полученная при кристаллизации такого сплава, – эвтектикой. Кристаллизацию эвтектического сплава можно описать следующей схемой:
Таким образом, эвтектика состоит из двух фаз – свинца и сурьмы. Структура сплава после окончательного затвердевания – эвтектика (рис. 3.6, б), которая является структурной составляющей.
Сплавы, расположенные слева от эвтектического, называются доэвтектическими, а расположенные справа – заэвтектическими. Первичная кристаллизация таких сплавов начинается с выделения избыточной фазы – фазы, содержание которой в сплаве больше, чем в сплаве эвтектического состава. Для рассматриваемой системы избыточной фазой является компонент. Таким образом, у доэвтектических сплавов избыточной фазой будет свинец (его содержание в них больше 87%), а у заэвтектических – сурьма (ее содержание в этих сплавах превышает 13%).
Кристаллизацию доэвтектических сплавов рассмотрим па примере сплава с 5% Sb и 95% Pb (см. рис. 3.4, б). До точки 1 сплав находится в жидком состоянии. В точке 1
Рис. 3.6. Структура доэвтектического (а), эвтектического (б) и заэвтектического (в) сплавов системы «Рb – Sb»
начинается кристаллизация сплава с выделением из жидкости кристаллов Рb. Этот процесс проходит в интервале температур 1–2 (участок 1–2 на кривой охлаждения). В указанном интервале температур система имеет одну степень свободы (К = 2 – компоненты Sb и Рb, Ф = 2 – твердая и жидкая фазы, следовательно, С = К- Ф+1 = = 2-2 + 1), т.е. возможно понижение температуры без изменения фазового состава. При охлаждении в этом интервале температур происходит изменение химического состава жидкой фазы: поскольку из жидкости выделяется свинец, в ней повышается содержание сурьмы. В точке 2, как показывают результаты химического анализа, в жидкой фазе содержится 13% Sb и 87% Рb (см. рис. 3.4, г). При температуре 246 °С (см. табл. 3.1) состав оставшейся жидкости соответствует эвтектическому. Кристаллизация осуществляется по эвтектическому механизму, т.е. при постоянной температуре и с одновременным выделением из жидкости двух твердых фаз – кристаллитов Sb и Рb (участок 2–2′ кривой охлаждения). После окончания кристаллизации (точка 2′ на кривой охлаждения) сплав охлаждается в твердом состоянии. Структура этого сплава после затвердевания состоит из зерен свинца и эвтектики (рис. 3.6, а). Аналогично протекает процесс кристаллизации всех доэвтектических сплавов данной системы.
Кристаллизация заэвтектичесих сплавов (на примере сплава III – 75% РЬ, 25% Sb, см. рис. 3.4, д и 3.5, 6) протекает аналогично доэвтектическим. Отличие заключается в том, что в интервале температур 1–2 диаграммы состояния (участок 2–2′ кривой охлаждения) из жидкости выделяются зерна сурьмы, а не свинца, как в первом сплаве. После окончательного затвердевания структура этого сплава состоит из зерен сурьмы и эвтектики (рис. 3.6, в).
Для сплавов данного типа возможна ликвация по плотности. Ликвация – неоднородность химического состава и соответственно свойств по объему сплава.
В процессе кристаллизации из жидкости выделяются кристаллы с плотностью, отличной от плотности жидкости. Это приводит к тому, что кристаллы либо всплывают, если их плотность меньше плотности жидкости, либо оседают на дно, если их плотность превышает плотность жидкости. В результате слиток получается неоднородным по составу и свойствам. Для предупреждения этого в процессе кристаллизации сплавы интенсивно перемешивают.
Видео:ДИАГРАММА СОСТОЯНИЯ ЖЕЛЕЗО-ЦЕМЕНТИТ, железо-углерод, Fe+Fe3CСкачать
Диаграммы состояния. Примеры решения
Видео:Диаграмма состояния сплавов системы «железо-углерод»Скачать

Задание 1
- Описать все превращения по диаграмме(название диаграммы, описание всех
точек, линий, фаз и структур). - Определить с помощью правила отрезков:
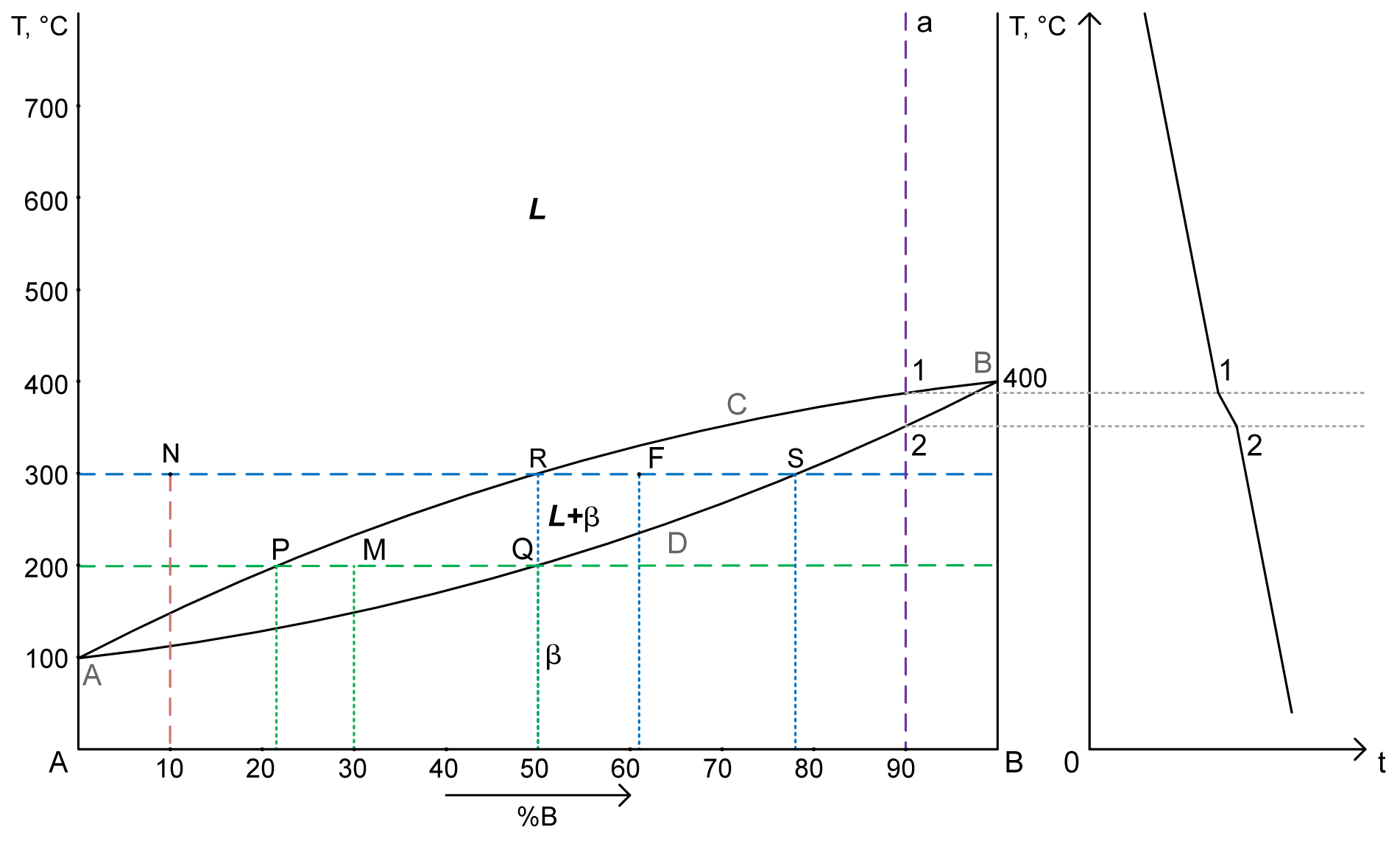
a. структуру сплава с 20%В при Т= 400°C
b. химический состав сплава по структуре Qβ= 33%, Qα= 67% при Т= 200°C
Определить химический состав найденных (задание а) и заданных (заданиеb) фаз. - Начертить кривую охлаждения для сплава содержащего15%В.
- Определить число степеней свободы для сплава с 30%В при Т= 300°C
Видео:Фазы в сплавах "железо-углерод" | Матвед 3Скачать

Решение
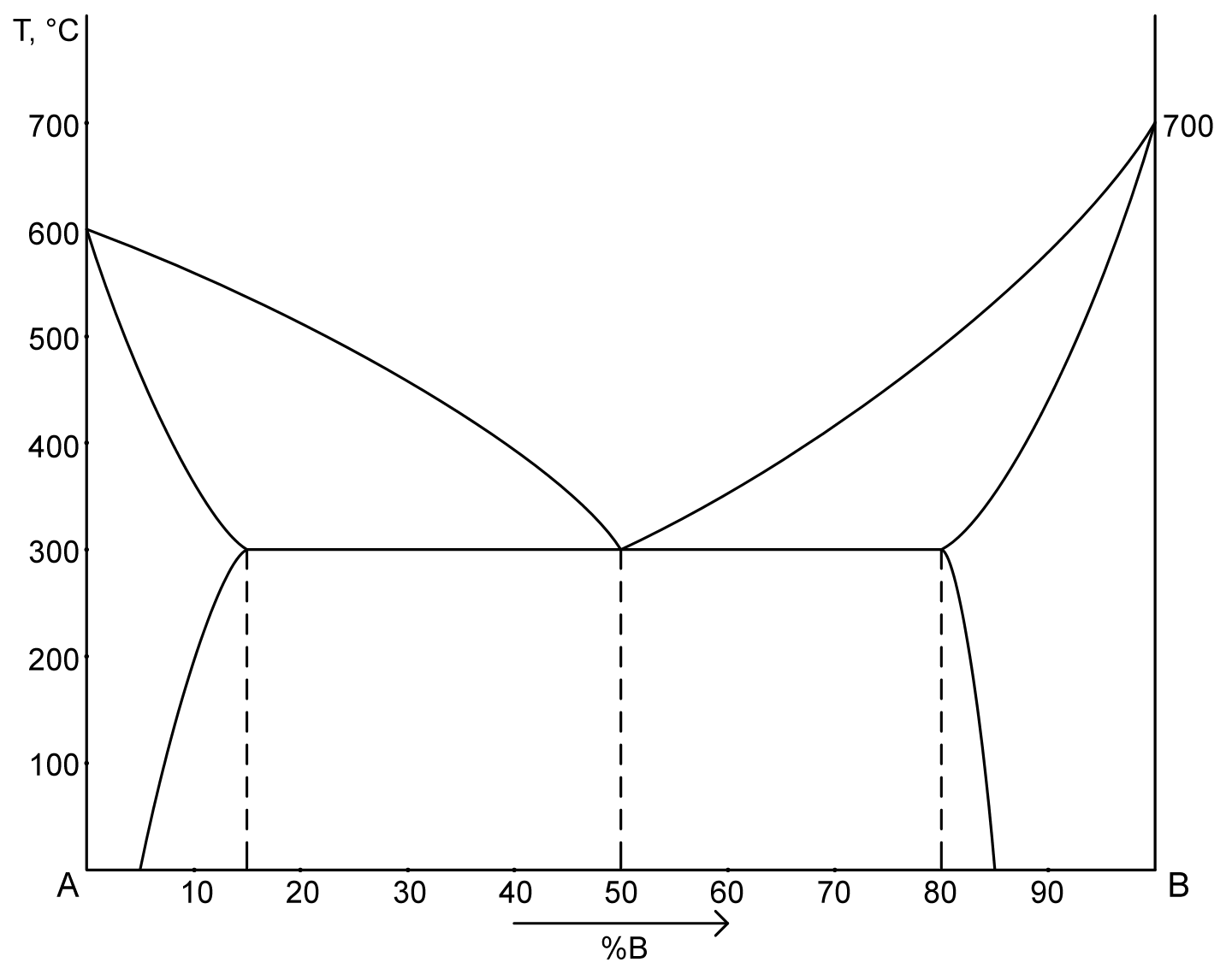
1. Диаграмма состояния сплавов, испытывающих фазовые превращения в твердом состоянии.
- A – температура плавления компонента A
- B – температура плавления компонента B
- L – жидкость
- α – кристаллы твердого раствора A
- β – кристаллы твердого раствора B
DF – линия предельной растворимоси компонента B в A
EG – линия предельной растворимоси компонента A в B
2. a) Структура сплава 20%В при Т= 400°C – точка M.
PM – твердый раствор α: 7% B => 93% A. Cα= 7% B+ 93% A
MQ – жидкость: 40% B => 60% A. Cж= 40% B+ 60% A
Qж= 100%-60,6% = 39,4% (Или: (PM/PQ)·100% = (20-7)/(40-7)·100% = 39,4%)
b) химический состав сплава по структуре Qβ= 33%, Qα= 67% при Т= 200°C – точка R.
B = 10+24=34% => A = 66%
3. Кривая охаждения для сплава 15%В – a
4. Число степеней свободы для сплава с 30%В при Т= 300°C – точка T.
C = 2-3+1 = 0 (компоненты (A, B) – фазы (α, β, эвтектика) + 1)
Видео:Урок 109 (осн). Задачи на вычисление количества теплотыСкачать

Задание 2
- Описать все превращения по диаграмме(название диаграммы, описание всех
точек, линий, фаз и структур). - Определить с помощью правила отрезков:
a. структуру сплава с 30%В при Т= 200°C
b. химический состав сплава по структуре Qβ= 40%, Qж= 60% при Т= 300°C
Определить химический состав найденных (задание а) и заданных (заданиеb) фаз. - Начертить кривую охлаждения для сплава содержащего 90%В.
- Определить число степеней свободы для сплава с 10%В при Т= 300°C
Видео:2 5 Фазовые превращения, диаграмма состояния веществаСкачать

Решение
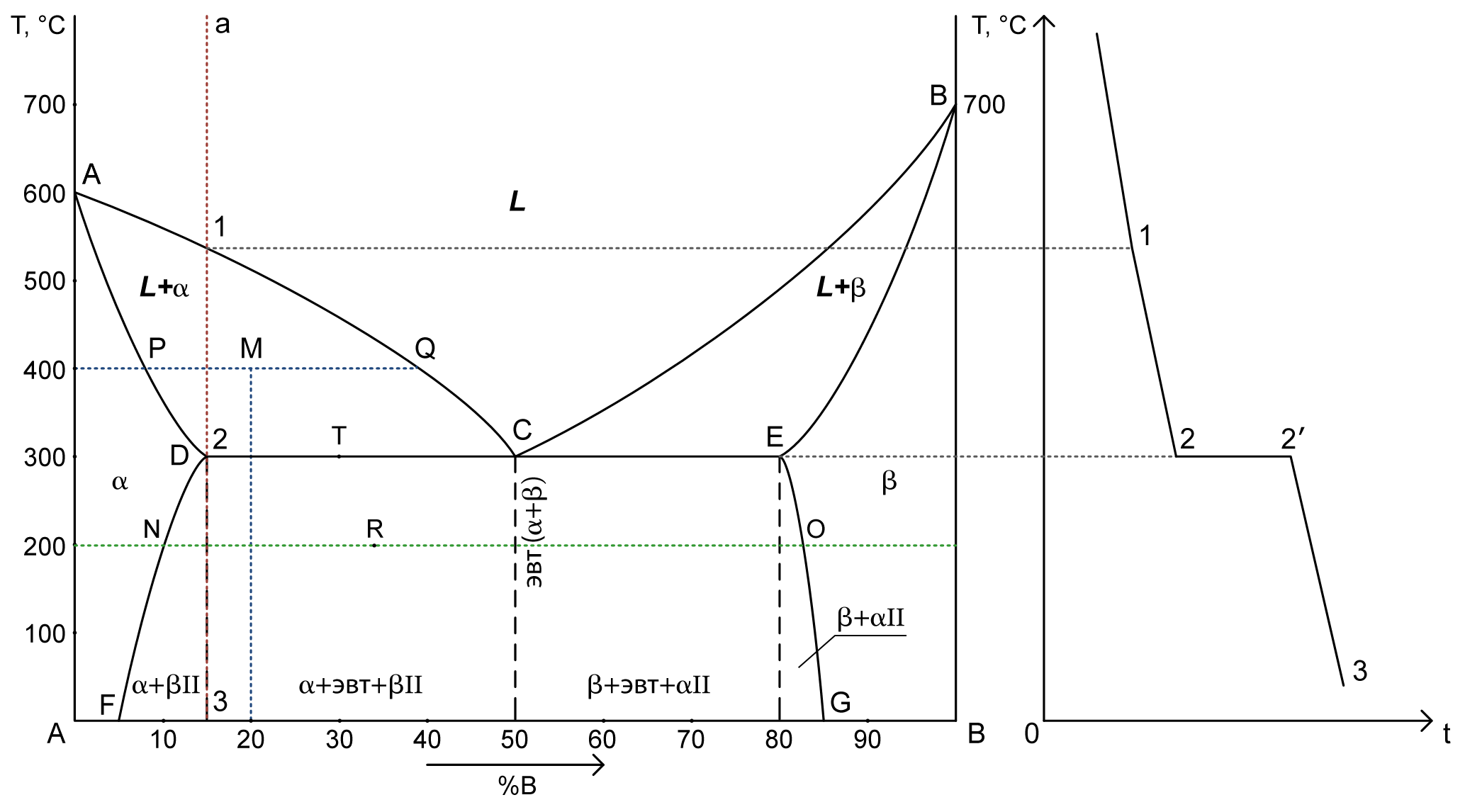
1. Диаграмма состояния сплавов с неограниченной растворимостью в твердом состоянии.
- A – температура плавления компонента A
- B – температура плавления компонента B
- L – жидкость
- β – кристаллы твердого раствора
2. a) Структура сплава 30%В при Т= 200°C – точка M.
PM – жидкость: 21% B => 79% A. Cж= 21% B+ 79% A
MQ – кристаллы твердого раствора: 50% B => 50% A. Cтв= 50% B+ 50% A
Qтв= 100%-69% = 31% (Или: (PM/PQ)·100% = (30-21)/(50-21)·100% = 31%)
b) химический состав сплава по структуре Qβ= 40%, Qж= 60% при Т= 300°C – точка F.
B = 50+11=61% => A = 39%
3. Кривая охаждения для сплава 90%В – a
4. Число степеней свободы для сплава с 10%В при Т= 300°C – точка N.
C = 2-1+1 = 2 (компоненты (A, B) – фазы (жидкость) + 1)
Видео:Диаграмма "железо-углерод". Кривые охлаждения. Лабораторная работаСкачать

Диаграмма состояния сплавов типа «смесь».
Приведем построение этой диаграммы на примере системы свинец—сурьма (Pb—Sb). Кривые охлаждения компонентов и сплавов представлены на рис. 9.4. Критические точки для чистых металлов и сплавов приведены в табл. 9.1.
Критические точки сплавов системы Pb—Sb
Химический состав, % масс
Температура кристаллизации, °С (критические точки)
На основании анализа кривых охлаждения (см. рис. 9.4 и табл. 9.1) построим диаграмму состояния Pb—Sb (рис. 9.5).
Линия диаграммы АВС, выше которой существует только жидкая фаза, называется линией ликвидус.
Линия диаграммы DBE, ниже которой существует только твердая фаза, называется линией солидус.
Анализ кривых охлаждения показал:
- • чистые металлы свинец и сурьма кристаллизуются при постоянной температуре;
- • кристаллизация всех сплавов, кроме одного (его состав — 87 % РЬ, 13 % Sb), протекает в интервале температур от линии ликвидус до линии солидус;
Рис. 9.4. Кривые охлаждения сплавов системы Pb-Sb
• сплав, химический состав которого 87 % РЬ, 13 % Sb, кристаллизуется при постоянной температуре и самой низкой температуре.
Этот наиболее легкоплавкий сплав системы называется эвтектическим сплавом, а его структура — эвтектикой. Особенностью эвтектического сплава является механизм его кристаллизации: жидкость кристаллизуется (затвердевает) с одновременным выделением свинца и сурьмы. Эвтектическое превращение можно описать следующим образом: Ж-»Э [Pb + Sb]. Таким образом, эвтектика — смесь, она состоит из двух фаз — свинца и сурьмы. Эвтектика является структурной составляющей.
Сплавы, расположенные слева от эвтектического, называются доэвтектиче- скими, а расположенные справа — заэвтектическими. Первичная кристаллизация таких сплавов начинается с выделения избыточной фазы — фазы, содержание которой в сплаве больше, чем в сплаве эвтектического состава. Таким образом, у доэвтектических сплавов избыточной фазой будет свинец (его содержание в них больше 87 %), а у заэвтектических — сурьма (ее содержание в этих сплавах превышает 13 %).
Кристаллизация доэвтектических сплавов начинается с выделения свинца, заэвтектических — с выделения сурьмы, т.е. избыточной фазы. По мере выделения из жидкости избыточной фазы ее состав меняется. У доэвтектических сплавов в ней увеличивается количество сурьмы за счет выделения из жидкости свинца, у заэвтектических — наоборот, увеличивается количество свинца. По мере охлаждения состав жидкости, таким образом, стремится к эвтектическому. При температуре 246 °С происходит окончательное затвердевание всех сплавов (см. табл. 9.1). При этой температуре состав жидкости любого сплава соответствует эвтектическому, и жидкость затвердевает по эвтектическому механизму, образуя смесь.
Таким образом, структура доэвтектических сплавов в системе Pb—Sb состоит из кристаллов свинца и эвтектики (РЬ + Э[РЬ + Sb]), а заэвтектических сплавов — из кристаллов сурьмы и эвтектики (Sb + Э[Pb + Sb]), что и показано на диаграмме состояния (рис. 9.5, а). Диаграмма, на которой указана структура сплавов, называется структурной диаграммой. Диаграмма, на которой указаны только фазы без описания структур, называется фазовой диаграммой (рис. 9.5, б). Напомним, что эвтектика состоит из двух фаз (Э[РЬ + Sb]). Схематично соответствующие структуры показаны на рис. 9.6.
Рис. 9.5. Диаграмма состояния системы РЬ—Sb: а — структурная; б — фазовая
Диаграммы состояния позволяют проводить анализ состояния сплавов. Он заключается в определении фазового состав сплава, химического состава каждой фазы (т.е. содержание в них компонентов), весового соотношения фаз (сколько весит каждая фаза) для любого сплава и при всех температурах его существования. Это выполняется по-разному в однофазных и двухфазных областях.
В однофазной области вес фазы равен весу сплава, а ее химический состав соответствует составу сплава. Так, при температуре t сплав I находится в жидком состоянии, т.е. имеет однофазную структуру (см. рис. 9.5, б). Состав жидкости и сплава определяется проекцией точки а на ось концентраций (72 % Sb и 28 % РЬ).
Этим приемом нельзя пользоваться при анализе состояния сплавов в двухфазных областях, поскольку при изменении температуры химический состав фаз и их масса не остаются постоянными.
Анализ состояния сплавов в двухфазных областях выполняют следующим образом (см. рис. 9.5, б). Через точку Ь, характеризующую положение сплава на диаграмме, проводят горизонталь — коноду — до пересечения с линиями диаграммы, ограничивающими двухфазную область, в которой лежит заданная точка (точка с — пересечение коноды с границей однофазной области существования жидкой фазы; точка d — твердой).
Фазовый состав сплава при данной температуре определится фазами тех однофазных областей, с которыми пересекается конода. В данном случае фазовый состав сплава — это жидкость (точка с) и сурьма (точка d).
Химический состав фаз соответствует проекциям точек пересечения коноды и линий диаграммы состояния на ось концентраций. Каждая проекция показывает состав той фазы, с которой граничит точка пересечения. Так, точка с’ определяет концентрацию компонентов в жидкой фазе (44 % Sb и 56 % РЬ), а точка d’ — концентрацию компонентов в твердой фазе (это чистый компонент — Sb).
Для определения массы фаз пользуются правилом рычага. В любой точке, т.е. при любой температуре, общая масса сплава соответствует длине коноды — отрезку cd. Количество соответствующей фазы определяется противолежащим отрезком: масса жидкости — отрезком bd, а твердой фазы — отрезком cb.
Для сплавов типа «смеси» характерна ликвация по плотности. Ликвация — это неодинаковость химического состава по объему сплава. В процессе кристаллизации из жидкости выделяются кристаллы с плотностью, отличной от плотности жидкости, что приводит к тому, что кристаллы либо всплывают, если их плотность меньше плотности жидкости, либо оседают на дно, если их плотность превышает плотность жидкости. В результате слиток получается неоднородным по составу и свойствам. Для предупреждения этого явления в процессе кристаллизации сплавы интенсивно перемешивают.
📺 Видео
3) Имитация термообработки, просто икрасивоСкачать

Диаграмма сплавов Железо углерод ЛекцияСкачать

Определение формулы органических соединений. 1 часть. Практическая часть - решение задачи. 9 класс.Скачать

Установление эмпирической и молек. формул по массовым долям элем., входящих в состав в-ва. 10 класс.Скачать

Лекция «Железоуглеродистые сплавы. Диаграмма состояния железо-углерод»Скачать

Математическое описание и расчёт кинетики фазовых превращений в сплавах железаСкачать

Диаграмма состояния железо-углеродСкачать

Материаловедение 05 11 2020Скачать
248) Диаграмма железо - углерод (материаловедение)Скачать

7. Правило фазСкачать

Органика. Решение задачи на определение состава вещества по продуктам его сгорания.Скачать

Успенская И. А. - Химическая термодинамика и кинетика - Фазовые диаграммыСкачать

Урок 119 (осн). Плавление и кристаллизация. Удельная теплота плавленияСкачать