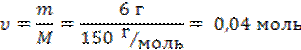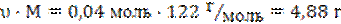Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Содержание
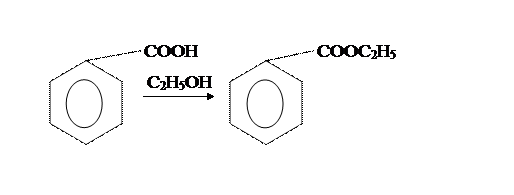
Этиловый эфир бензойной кислоты. Формула соединения и его названия. Основание выбора схемы синтеза соединенияСтраницы работыФрагмент текста работыМИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ РОССИЙСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ НЕФТИ И ГАЗА им. И.М. ГУБКИНА КАФЕДРА ОРГАНИЧЕСКОЙ ХИМИИ И ХИМИИ НЕФТИ по синтетическим методам органической химии «Этиловый эфир бензойной кислоты» Выполнил: студент группы ХТ-06-3 2.Теоретическая часть. 3 2.1. Формула соединения и его названия. 3 2.2. Физические свойства соединения. 3 2.3. Химические свойства соединения. 4 2.4. Применение соединения. 6 2.5. Методы получения этилбензоата. 6 2.6. Основание выбора схемы синтеза соединения. 7 3. Экспериментальная часть. 8 3.1. Расчет количеств исходных веществ по второй стадии. 8 3.1.1. Уравнение основной и побочной реакции. 8 3.1.2. Расчет и таблица характеристик и количеств исходных реагентов и продуктов реакции. 8 3.1.3. Описание синтеза [2] 9 3.1.4 Константы полученного соединения. 10 3.2. Расчет количеств исходных веществ по первой стадии. 10 3.2.1. Уравнение основной и побочной реакции. 10 3.2.2. Расчет и таблица характеристик и количеств исходных реагентов и продуктов реакции. 10 3.2.3. Описание синтеза [2] 11 3.2.5. Схема установки. 13 5. Используемая литература. 15 1. ВведениеПо окончанию лабораторного практикума по органической химии проводится литературный анализ. Целью литературного анализа является нахождение литературы по данному веществу, проведение синтеза вещества и анализ полученных результатов. Целью нашего синтеза является получение этилового эфира бензойной кислоты (6 г). Синтез проводится в две стадии (получение бензойной кислоты – первая стадия, получение этилового эфира бензойной кислоты – вторая стадия). 2. Теоретическая часть2.1. Формула соединения и его названияЭтиловый эфир бензойной кислоты (этилбензоат) 2.2. Физические свойства соединения
2.3. Химические свойства соединенияЭфиры – нейтральные и малоактивные соединения. Разбавленные кислоты, щелочи, металлический натрий и PCl5 на холоду на них не действует. [3] I. Реакции с участием эфирного кислорода: 1.1. Образование оксониевых соединений. Эфиры присоединяют кислоты к кислороду эфира за счет его неподеленных электронов: Образующиеся комплексные соли напоминают соли аммония. Оксониевые соли эфиров – обычные промежуточные продукты в их реакциях в присутствии кислот. [3] 1.2. Образование комплексных солей с различными солями:
II. Реакции сопровождающиеся гомолизом α- С-Н связи: 2.1. Взаимодействие с хлором:
2.2. Взаимодействие с нитрилами:
2.3. Взаимодействие с магний органическими соединениями:
2.4. Образование гидроперекиси:
III. Реакции расщепления по эфирному кислороду: 3.1. Металлический натрий при нагревании расщепляет эфиры: 3.2. Ацидолиз. Концентрированные кислоты (серная, йодистоводородная), а также некоторые другие реагенты (хлорное железо в уксусном ангидриде, ацетилтозилаты) расщепляют эфиры по механизму SN1 или SN2:
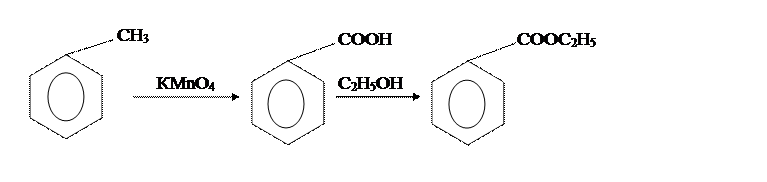
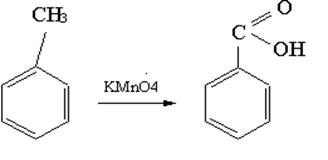
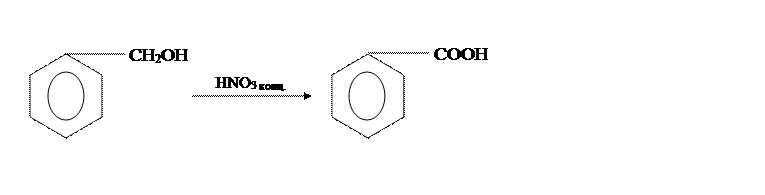
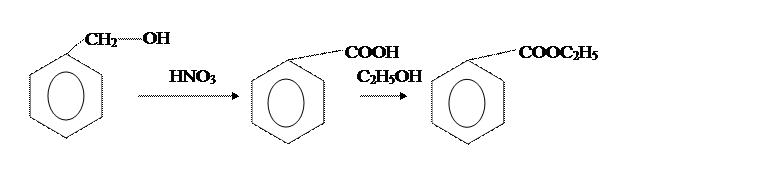
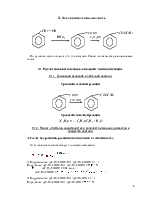
2.4. Применение соединенияЭтилбензоат применяют в парфюмерии. Используют как растворитель эфиров целлюлозы. В медицине его употребляют для усиления сердечной деятельности. [4] 2.5. Методы получения этилбензоатаМетоды получения этилбензоата отличаются только различными способами получения бензойной кислоты и условиями провидения синтеза. Так, в [6] бензойную кислоту получают из толуола и КМnО4, по реакции:В [2] бензойную кислоту получают из бензилового спирта и концентрированной НNO3, |
по реакции:
Вторая стадия отличается только способами провидения аппаративного оформления этерификации бензойной кислоты этиловым спиртом.
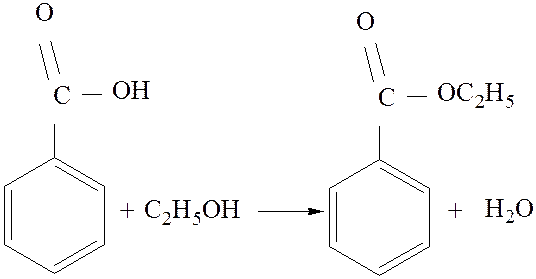 |
2.6. Основание выбора схемы синтеза соединения
Из приведенных методик наиболее оптимальна вторая. [2]
1) С учетом ограниченности времени, эта методика меньше времени занимает при ее проведении.
2) В лаборатории имеются все необходимые реактивы и приборы для проведения данной методики.
3. Экспериментальная часть
По условию нужно получить 6 г этилбензоата. Расчет по обеим стадиям начинаем с конца.
3.1. Расчет количеств исходных веществ по второй стадии.
3.1.1. Уравнение основной и побочной реакции.
Уравнение основной реакции
Уравнение побочной реакции
3.1.2. Расчет и таблица характеристик и количеств исходных реагентов и продуктов реакции.
А. Расчет по уравнению реакции (для получения 6 г этилбензоата):
6 г этилбензоата соответствует количество вещества:
По условию: υ(C6H5-COOC2H5) : υ(C6H5-COOH) = 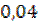
m(C6H5-COOH) =
По условию: υ(C6H5-COOC2H5) : υ(C2H5-OH) = 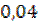
m(C2H5-OH) = 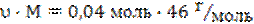
Б. Расчет количеств веществ по практикуму:
В практикуме Агрономова для получения 10 г этилбензоата используется 10 г бензойной кислоты, 26 г (33мл) этилового спирта, 1 мл H2SO4 (d=1,84):
Для синтеза 6 г этилбензоата требуется бензойной кислоты:
Для синтеза 6 г этилбензоата требуется этилового спирта:
Бензойная кислота и этанол уравнение
Установите соответствие между реагирующими веществами и продуктом, который образуется при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | ПРОДУКТ ВЗАИМОДЕЙСТВИЯ | ||
| A | Б | В | Г |
A. Происходит реакция этерификации — продуктом является этилбензоат. (5)
Б. Метилфенилкетон можно получить действием бензола в присутствии кислоты Льюиса на ацетилхлорид (реакция Фриделя–Крафтса). (6)
В. Диизопропиловый эфир получают дегидратацией изопропилового спирта в присутствии серной кислоты (2)
Г. Хлорангидрид уксусной кислоты при взаимодействии с фенолом даст соответствующий сложный эфир — фенилацетат. (3)



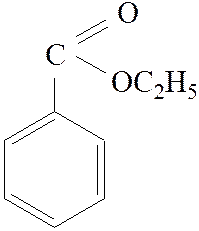
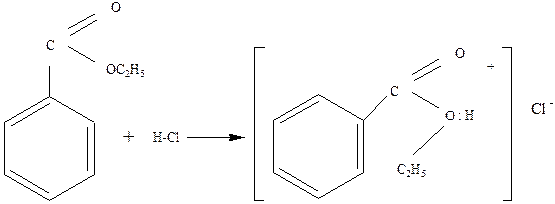
 [4]
[4]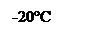
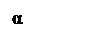
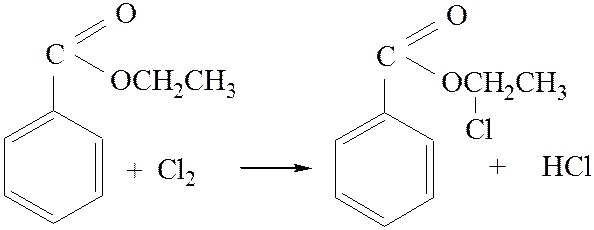 [4]
[4]
 [4]
[4]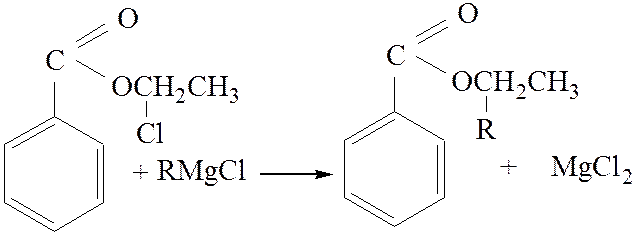 [4]
[4]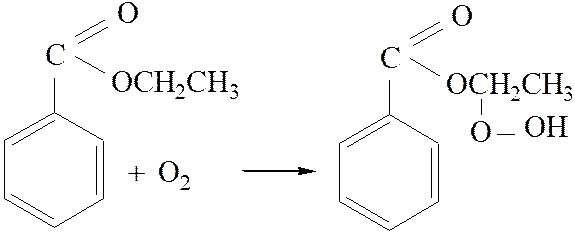 [4]
[4]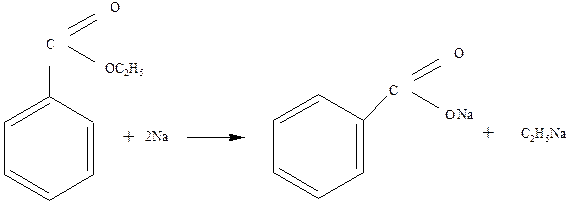
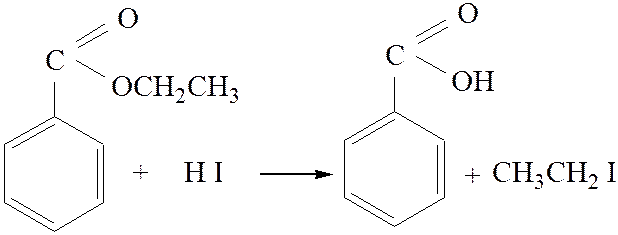 [3]
[3]