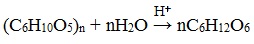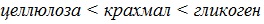Полисахариды – это природные высокомолекулярные углеводы, макромолекулы которых состоят из остатков моносахаридов.
Полисахариды – высокомолекулярные несахароподобные углеводы, содержащие от десяти до сотен тысяч остатков моносахаридов (обычно гексоз), связанных гликозидными связями.
Основные представители — крахмал и целлюлоза — построены из остатков одного моносахарида — глюкозы. Крахмал и целлюлоза имеют одинаковую молекулярную формулу
но совершенно различные свойства. Это объясняется особенностями их пространственного строения.
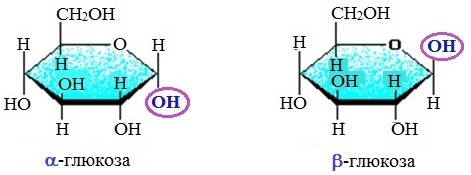
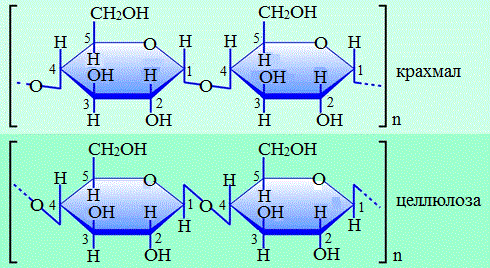
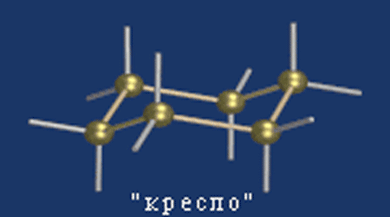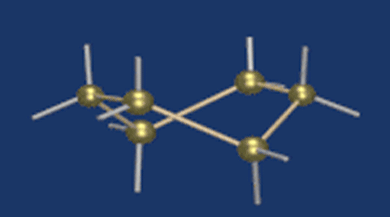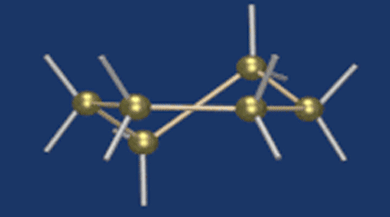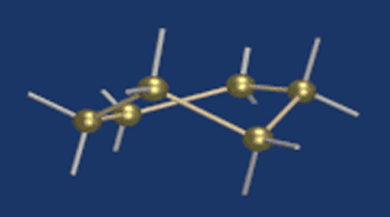
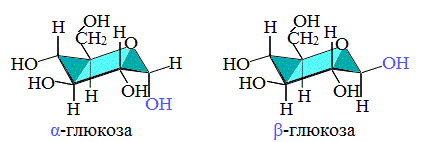
Крахмал состоит из остатков a-глюкозы, а целлюлоза – из b-глюкозы, которые являются пространственными изомерами и отличаются лишь положением одной гидроксильной группы (выделена цветом):
С учетом пространственного строения шестичленного цикла
формулы этих изомеров имеют вид:
К важнейшим полисахаридам относится также гликоген (С6Н10О5)n, образующийся в организмах человека и животных в результате биохимических превращений из растительных углеводов. Как и крахмал, гликоген состоит из остатков a-глюкозы и выполняет подобные функции (поэтому часто называется животным крахмалом).
Учебный фильм «Углеводы. Полисахариды»
- Биологическая роль полисахаридов
- Физические свойства
- Химические свойства полисахаридов
- Различия в строении и свойствах крахмала и целлюлозы
- Общее итоговое уравнение гидролиза полисахаридов?
- Уравнение гидролиза сахарозы сахаразой?
- Уравнение гидролиз сульфата меди?
- Напишите уравнения гидролиза в молекулярном и ионном виде всех ступеней гидролиза для раствора фосфата натрия?
- Уравнение гидролиза NH4NO2?
- Уравнение гидролиза AlCl3?
- Уравнение гидролиза NaCl?
- Чем отличаются реакции гидролиза от реакции гидратации?
- ZnSO4, NH4NO3, CH3COONa напишите краткое и полное ионно — молекулярное уравнение гидролиза, а так же молекулярное уравнение гидролиза?
- Уравнение гидролиза солей в молекулярной и ионной формах совместного гидролиза солей FeBr2 + NaCO3?
- Уравнения гидролиза глюкозы?
- § 15. Дисахариды и полисахариды
Биологическая роль полисахаридов
Полисахариды необходимы для жизнедеятельности животных и растительных организмов. В живой природе они выполняют важные биологические функции:
- структурных компонентов клеток и тканей;
- энергетического резерва;
- защитных веществ.
Они являются одним из основных источников энергии, образующейся в результате обмена веществ организма. Принимают участие в иммунных процессах, обеспечивают сцепление клеток в тканях. Являются основной массой органического вещества в биосфере.
Структурные полисахариды придают клеточным стенкам прочность.
Водорастворимые полисахариды не дают клеткам высохнуть.
Резервные полисахариды по мере необходимости расщепляются на моносахариды и используются организмом.
Физические свойства
Полисахариды — аморфные вещества, не растворяются в спирте и неполярных растворителях, растворимость в воде варьируется. Некоторые растворяются в воде с образованием коллоидных растворов (амилоза, слизи, пектовые кислоты, арабин), могут образовывать гели (пектины, альгиновы кислоты, агар-агар) или вообще не растворяться в воде (клетчатка, хитин).
Химические свойства полисахаридов
Для полисахаридов наибольшее значение имеют реакции гидролиза и образование производных за счет реакций макромолекул по спиртовым ОН-группам.
Гидролиз полисахаридов
Гидролиз полисахаридов происходит в разбавленных растворах минеральных кислот (или под действием ферментов). При этом в макромолекулах разрываются связи, соединяющие моносахаридные звенья – гликозидные связи (аналогично гидролизу дисахаридов). Реакция гидролиза полисахаридов является обратной процессу их образования из моносахаридов.
Полный гидролиз полисахаридов приводит к образованию моносахаридов (целлюлоза, крахмал и гликоген гидролизуются до глюкозы):
При неполном гидролизе образуются олигосахариды (в том числе, дисахариды).
Способность полисахаридов к гидролизу увеличивается в ряду:
Гидролиз крахмала и целлюлозы до глюкозы («осахаривание») и ее брожение используются в производстве этанола, молочной, масляной и лимонной кислот, ацетона, бутанола.
Образование производных
Образование производных (главным образом, сложных и простых эфиров) полисахаридов происходит в результате реакций по спиртовым ОН-группам, содержащимся в каждом структурном звене (3 группы ОН на одно моносахаридное звено): [С6Н7О2(ОН)3]n.
Различия в строении и свойствах крахмала и целлюлозы
1. Содержат остатки разных форм циклической глюкозы:
крахмал – остатки α–глюкозы;
целлюлоза – остатки β-глюкозы.
2. Содержат разное число структурных звеньев – остатков глюкозы:
крахмал – до нескольких тысяч (Мr – до 1 млн);
целлюлоза – до 40 тыс. (Мr – до 20 млн).
3. Между остатками глюкозы образуются различные связи:
в крахмале – α–1,4- и α–1,6-гликозидные связи;
в целлюлозе — β-1,4-гликозидные связи.
4. Макромолекулы имеют различную структуру:
крахмал – разветвленные и неразветвленные молекулы, компактно свернутые;
целлюлоза – только неразветвленные молекулы, имеют вид нитей, так как форма остатков β-глюкозы исключает спирализацию.
5. Характер межмолекулярных взаимодействий:
в крахмале макромолекулы имеют компактную форму, водородные связи между ними почти не образуются;
в целлюлозе между молекулами нитевидной формы образуются очень прочные водородные связи (в которых участвуют свободные гидроксильные группы), нити объединяться в пучки, пучки в волокна. Поэтому в воде, спирте, эфире целлюлоза не растворяется и не набухает, как крахмал.
6. Как пищевой продукт:
Крахмал – продукт питания, так как в организмах человека и животных есть ферменты, расщепляющие α–1,4- и α–1,6-гликозидные связи.
Целлюлоза не является продуктом питания человека и большинства животных, так как в их организмах нет ферментов, расщепляющих более прочные β-1,4-гликозидные связи.
Жвачные животные и кролики способны усваивать целлюлозу при посредстве содержащихся в их организме бактерий.
Общее итоговое уравнение гидролиза полисахаридов?
Химия | 5 — 9 классы
Общее итоговое уравнение гидролиза полисахаридов.
(C6H10O5)n + nH2O = nC6H12O6.
Уравнение гидролиза сахарозы сахаразой?
Уравнение гидролиза сахарозы сахаразой.
Уравнение гидролиз сульфата меди?
Уравнение гидролиз сульфата меди.
Напишите уравнения гидролиза в молекулярном и ионном виде всех ступеней гидролиза для раствора фосфата натрия?
Напишите уравнения гидролиза в молекулярном и ионном виде всех ступеней гидролиза для раствора фосфата натрия.
Уравнение гидролиза NH4NO2?
Уравнение гидролиза NH4NO2.
Уравнение гидролиза AlCl3?
Уравнение гидролиза AlCl3.
Уравнение гидролиза NaCl?
Уравнение гидролиза NaCl?
Чем отличаются реакции гидролиза от реакции гидратации?
Чем отличаются реакции гидролиза от реакции гидратации?
И что между ними общего?
ZnSO4, NH4NO3, CH3COONa напишите краткое и полное ионно — молекулярное уравнение гидролиза, а так же молекулярное уравнение гидролиза?
ZnSO4, NH4NO3, CH3COONa напишите краткое и полное ионно — молекулярное уравнение гидролиза, а так же молекулярное уравнение гидролиза.
Уравнение гидролиза солей в молекулярной и ионной формах совместного гидролиза солей FeBr2 + NaCO3?
Уравнение гидролиза солей в молекулярной и ионной формах совместного гидролиза солей FeBr2 + NaCO3.
Уравнения гидролиза глюкозы?
Уравнения гидролиза глюкозы.
На этой странице вы найдете ответ на вопрос Общее итоговое уравнение гидролиза полисахаридов?. Вопрос соответствует категории Химия и уровню подготовки учащихся 5 — 9 классов классов. Если ответ полностью не удовлетворяет критериям поиска, ниже можно ознакомиться с вариантами ответов других посетителей страницы или обсудить с ними интересующую тему. Здесь также можно воспользоваться «умным поиском», который покажет аналогичные вопросы в этой категории. Если ни один из предложенных ответов не подходит, попробуйте самостоятельно сформулировать вопрос иначе, нажав кнопку вверху страницы.
W(C) = 0, 9231 w(H) = 0, 0769 D / H₂ = 39 M(C) = 12 г / моль M(H) = 1 г / моль M(H₂) = 2 г / моль M(CₓHy) = M(H₂) * D xM(C) = M(CₓHy)w(C) = M(H₂)Dw(C) x = M(H₂)Dw(C) / M(C) аналогично y = M(H₂)Dw(H) / M(H) x = 2 * 39 * 0, 9231 / 12 = 6 y = 2 * 39 * 0..
Это электронная формула калия (K).
Соответствую перечню — ответ — а.
Ответ на фото. Будут вопросы — задавай.
Метан СН₄ и углекислый газ СО₂ — газообразные соединения углерода. Метан относится к классу органических веществ, а так же к классу летучих водородных соединений ; ауглекислый газ — неорганических, а так же к классу оксидов. Сходство : Химические с..
§ 15. Дисахариды и полисахариды
Наряду с моносахаридами в природе широко распространены и дисахариды. Это всем хорошо известная сахароза (тростниковый или свекловичный сахар), лактоза (молочный сахар), мальтоза (солодовый сахар).
Термин «дисахарид» красноречиво говорит о том, что в молекулах этих органических соединений между собой связаны два остатка моносахаридов, которые можно получить гидролизом (разложением водой) молекулы дисахарида.
| Дисахариды — это углеводы, которые гидролизуются с образованием двух молекул моносахаридов. |
При образовании молекулы дисахарида происходит отщепление одной молекулы воды:
поэтому молекулярная формула дисахаридов С12Н22О11.
Как вы уже знаете, образование наиболее известного дисахарида сахарозы происходит в клетках растений под действием ферментов. Однако химики научились осуществлять многие реакции, которые являются частью процессов, происходящих в живой природе. В 1953 г, французским химиком Р. Лемье впервые в лабораторных условиях был осуществлен синтез сахарозы, который современники назвали «покорением Эвереста органической химии».
В промышленности сахарозу получают из сока сахарного тростника (содержание 14—16%), сахарной свеклы (16—21%) и некоторых других растений, например канадского клена, земляной груши (рис. 70).
Рис. 70.
Растения-сахароносы:
1 — земляная груша (топинамбур); 2 — сахарный тростник; 3
канадский клен; 4 — сахарная свекла
Не только сладкоежки, но и любой из вас знает, что сахароза представляет собой кристаллическое хорошо растворимое в воде вещество и имеет сладкий вкус.
Тростниковый сахар был известен людям достаточно давно. Родиной сахарного тростника считается Индия. В соке этого растения содержится углевод сахароза, который мы привычно называем сахаром. Белые твердые куски, похожие на камни, использовали не только для придания сладкого вкуса пище, но и как лекарственное средство.
В XII в. сахарный тростник стали возделывать на Сицилии, а в XVI в. он был завезен на Кубу и другие острова Карибского моря.
«Главной сладостью» в европейских государствах с давних времен был мед и продукты на его основе. На первых порах сахар был заморской диковинкой и непозволительной роскошью. Потребность в новом продукте резко возросла, когда в европейских странах в моду вошли чай и кофе. Естественно стали предприниматься многочисленные попытки получения сахара из растений, произрастающих в более холодных климатических условиях Европы. Таким растением оказалась сахарная свекла.
Производство сахара из свеклы связано с именем А. Маргграфа, немецкого химика и металлурга. А. Маргграф был одним из первых исследователей, который применил в химических исследованиях микроскоп, с помощью которого и обнаружил в 1747 г. кристаллы сахара в свекольном соке.
Из молока млекопитающих еще в XVII в. был получен кристаллический молочный сахар (лактоза). Лактоза менее сладкий дисахарид, чем сахароза.
А теперь познакомимся с углеводами более сложного строения — полисахаридами. Термин «полисахариды» логично приводит нас к выводу о том, что в молекулах этих углеводов между собой связано множество остатков моносахаридов, в первую очередь глюкозы.
| Полисахариды — это углеводы, которые гидролизуются с образованием множества молекул моносахаридов. Их относят к биополимерам. |
Общая схема гидролиза полисахаридов упрощенно может быть представлена так:
Сравним строение и свойства двух важнейших представителей полисахаридов — крахмала и целлюлозы.
Структурным звеном полимерных цепей этих полисахаридов, формула которых (С6Н10О5)л, являются остатки глюкозы. Чтобы записать состав структурного звена (С6Н10О5), необходимо из формулы глюкозы отнять молекулу воды.
Крахмал и целлюлоза имеют растительное происхождение и образуются из молекул глюкозы в результате реакции поликонденсации.
Для полисахаридов уравнение реакции поликонденсации и обратного ей процесса гидролиза условно можно записать так:
Степень полимеризации макромолекул крахмала (число структурных звеньев в макромолекуле полимера, обозначаемое индексом n в формуле вещества) меньше, чем у целлюлозы.
Молекулы крахмала имеют как линейное, так и разветвленное строение, а целлюлозы — только линейное строение.
В отличие от целлюлозы, крахмал дает синее окрашивание при взаимодействии с иодом (рис. 71). Это качественная реакция на крахмал.
Рис. 71.
Качественная реакция на крахмал
Различны и функции этих полисахаридов в растительной клетке. Крахмал играет роль запасного питательного вещества, а целлюлоза — структурную, строительную. Из целлюлозы построены стенки растительных клеток.
Рис. 72.
Применение целлюлозы:
1 — вата, марля и бинты; 2 — пластмасса (целлулоид); 3 — фотопленка; 4 — искусственные волокна и ткани; 5 — клей; 6 — порох; 7 — эмали и лаки; 8 — бумага и изделия из нее
Различно также использование целлюлозы (рис. 72) и крахмала (рис. 73) в промышленности. Образующуюся в результате гидролиза крахмала глюкозу применяют для производства медицинского и пищевого этилового спирта, используемого для приготовления ликероводочных изделий и лекарств. Этиловый спирт, полученный из целлюлозы, называют техническим и используют, например, как растворитель при производстве лакокрасочных материалов или для получения синтетических каучуков.
Рис. 73.
Применение крахмала:
1 — получение патоки; 2 — подкрахмаливание белья; 3 — приготовление киселей; 4 — производство этанола; 5 — выпечка кондитерских изделий
Технический спирт не предназначен для питья, он опасен для здоровья. Для того чтобы любители спиртного поостереглись применять его вовнутрь, в такой спирт добавляют специальные предупреждающие цветом и запахом добавки. Такой «помеченный» спирт называют денатуратом. Ежегодно от отравления фальшивой водкой, изготовленной с использованием технического спирта, в стране гибнет 50 ООО человек.